
【题目】氧化钴(Co2O3)粉体材料在工业、电子、电讯等领域都有着广阔的应用前景。某铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。由该矿石制备Co2O3的部分工艺流程如下:
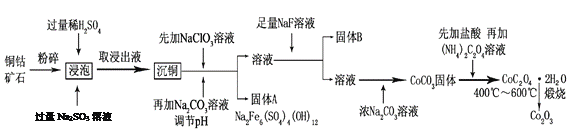
请回答下列问题:
(1)“浸泡”过程中,CoO(OH)可转化为CoSO4,请将该反应的化学方程式补充完整:
2CoO(OH)+2H2SO4+□_______=□CoSO4+□_______+□_______,_____________
(2)固体B的成分是______________________(填化学式)。
(3)向“沉铜”后的滤液中加入NaClO3溶液的主要目的是___________________;若上述流程中固、液分离均采用过滤操作,则共有________________处使用该操作。
(4)根据图1、图2分析:
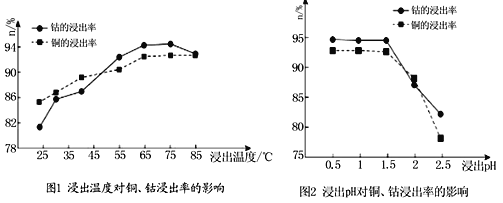
①矿石粉末浸泡的适宜条件应是________________________________。
②图2中铜、钴浸出率下降的可能原因是___________________________________。
(5)CoC2O4·2H2O在空气中高温煅烧得到Co2O3的化学方程式是_____________。
(6)LiCoO2可用于电动汽车的电池,其工作原理如右图所示,且电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为:LixC6+Li1-xCoO2 ![]() C6 +LiCoO2
C6 +LiCoO2
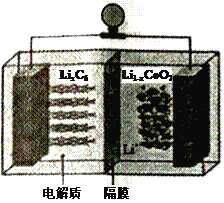
①放电时,Li+移动的方向为_________→___________。(填“ 左”或“ 右”)
②放电时正极的电极反应式为______________________________________。
【答案】 1 Na2SO3 2 1 Na2SO4 3 H2O CaF2、MgF2 将Fe2+氧化为Fe3+,再沉淀分离 6 温度:65℃~75℃、pH:0.5~1.5 pH升高后溶液中c(H+)浓度下降,使得溶解CoO(OH)、CoCO3、Cu2(OH)2CO3的能力下降 4 CoC2O4·2H2O+3O2![]() 2Co2O3+8CO2+8H2O 左 右 Li1-xCoO2+xLi++xe-= LiCoO2
2Co2O3+8CO2+8H2O 左 右 Li1-xCoO2+xLi++xe-= LiCoO2
【解析】(1)“浸泡”过程中,CoO(OH)可转化为CoSO4,根据流程图和氧化还原反应的规律,反应中Co的化合价降低,则亚硫酸钠中S的化合价升高,配平后的方程式为2CoO(OH)+2H2SO4+ Na2SO3=CoSO4+ Na2SO4+3H2O,故答案为:Na2SO3;Na2SO4;3H2O;
(2)某铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等,根据(1)的分析,浸出液中含有CoSO4、Na2SO4,以及硫酸铜、硫酸镁、硫酸亚铁和少量硫酸钙,经过沉铜后加入氯酸钠将亚铁离子氧化,调节pH沉淀铁离子,得到的溶液中加入氟化钠主要生成氟化钙和氟化镁沉淀,故答案为:CaF2、MgF2;
(3)向“沉铜”后的滤液中加入NaClO3溶液的主要目的是将Fe2+氧化为Fe3+,再沉淀分离;若上述流程中固、液分离均采用过滤操作,则共有6处使用了过滤,分别为浸泡后取浸出液、沉铜、调节pH沉铁、加入氟化钠沉淀钙离子和镁离子、加入浓碳酸钠沉钴、碳酸钴用盐酸溶解后加入草酸铵生成草酸钴沉淀,故答案为:将Fe2+氧化为Fe3+,再沉淀分离;6;
(4)①根据图像,矿石粉末浸泡时的浸出率最高的条件为:温度在65℃-75℃、pH在0.5-1.5,故答案为:温度:65℃-75℃、pH:0.5-1.5;
②根据图像,pH升高后溶液中c(H+)浓度下降,使得溶解CoO(OH)、CoCO3、Cu2(OH)2CO3的能力下降,导致铜、钴浸出率下降,故答案为:pH升高后溶液中c(H+)浓度下降,使得溶解CoO(OH)、CoCO3、Cu2(OH)2CO3的能力下降;
(5)CoC2O4·2H2O在空气中高温煅烧得到Co2O3,钴元素的化合价升高,被空气中的氧气氧化,同时草酸根被氧化氧化生成二氧化碳和水,反应的化学方程式为4CoC2O4·2H2O+3O2![]() 2Co2O3+8CO2+8H2O,故答案为:4CoC2O4·2H2O+3O2
2Co2O3+8CO2+8H2O,故答案为:4CoC2O4·2H2O+3O2![]() 2Co2O3+8CO2+8H2O;
2Co2O3+8CO2+8H2O;
(6)根据电池反应式LixC6+Li1-xCoO2![]() C6 +LiCoO2知,负极反应式为LixC6-xe-=C6+xLi+、正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,充电时,阴极、阳极反应式与负极、正极反应式正好相反,所以左侧是负极、右侧是正极。
C6 +LiCoO2知,负极反应式为LixC6-xe-=C6+xLi+、正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,充电时,阴极、阳极反应式与负极、正极反应式正好相反,所以左侧是负极、右侧是正极。
①放电时,Li+由负极通过隔膜移向正极,即移动的方向为左→右,故答案为:左;右;
②放电时,正极反应式为Li1-xCoO2+xLi++xe-=LiCoO2,故答案为:Li1-xCoO2+xLi++xe-= LiCoO2。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】危险化学药品的包装标签上印有警示标志,下列化学药品名称与警示标志对应正确的是( )
A.汽油—易燃品B.浓硫酸—易爆品
C.酒精—剧毒品D.浓硝酸—放射性物品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5 , 反应PCl5(g)PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表:下列说法正确的是( )
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50s的平均速率v(Cl2)=0.0016 molL﹣1min﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 molL﹣1 , 则该反应的△H<0
C.温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2 , 反应达到平衡前v(正)<v(逆)
D.温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2 , 达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂D.海域天然气水合物试采连续60天
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是重要的基础化工原料,广泛用于制药、染化。塑胶助剂等行业。某兴趣小组模拟PCl3直接氧化法制备POCl3,实验装置设计如下:

有关物质的部分性质如下表:
熔点/℃ | 沸点/℃ | 其他 | |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
回答下列问题:
(1)仪器a的名称是_____,装置A中发生反应的化学方程式为____________。
(2)B装置的作用除观察O2的流速之外。还有____________。
(3)C装置控制反应在60℃~65℃进行,其主要目的是____________。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
I.取xg产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至酸性。
II.向锥形瓶中加入0.1000mol/L的AgNO3溶液40.00mL,使Cl-完全沉淀。
III.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
IV.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是_______(填标号),滴定終点的现象为_____________。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②C1元素的质量百分含量为(列出算式)____________。
③步骤III加入硝基苯的目的是___,如无此操作,所测C1元素含量将会___(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小组利用下列装置检验草酸亚铁晶体受热分解的部分产物。
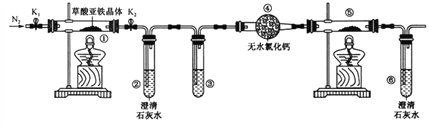
下列说法正确的是
A. 若③和⑤中分别盛放足量NaOH溶液和CuO,可检验生成的CO
B. 实验时只需要在装置①中反应结束后再通入N2
C. 若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气
D. 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,书写不正确的是( )
A.Ca(OH)2=Ca2++2OH-B.NaOH=Na++O2-+H+
C.HCl=H++Cl-D.KHCO3=K++HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。

Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________,B→C的反应条件为__________,C→Al的制备方法称为______________。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___________。
a.温度 b.Cl-的浓度 c.溶液的酸度
(3)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
Ⅱ.含铬元素溶液的分离和利用
(4)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com