乙醇是重要的化工原料和液体燃料,可以利用下列反应制取乙醇:
2CO
2(g)+6H
2(g) CH
3CH
2OH(g)+3H
2O(g)
(1)写出该反应的平衡常数表达式:K=______.
(2)请说明以CO
2为原料合成乙醇的优点是______(只要求写出一条).
(3)在一定压强下,测得该反应的实验数据如下表:
温度/℃CO2转化率/%
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
①该反应是______反应(填“吸热”或“放热”).
②一定条件下,若提高氢碳比[n(H
2)/n(CO
2)],则CO
2的转化率______;平衡常数K______.(填“增大”、“减小”、或“不变”)
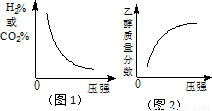
(4)在下图的坐标系中作图说明压强变化对该反应化学平衡的影响,并对图中横坐标、纵坐标的含义作必要的标注.

(5)一种乙醇燃料电池中发生的化学反应为:在酸性溶液中乙醇与氧作用生成水和二氧化碳.该电池的负极反应式为:
______.
(6)25℃、101kPa下,H
2(g)、C
2H
4(g)和C
2H
5OH(l)的燃烧热分别是285.8kJ?mol
-1、1411.0kJ?mol
-1和1366.8kJ?mol
-1,请写出由C
2H
4(g)和H
2O(l)反应生成C
2H
5OH(l)的热化学方程式______.


 ;
;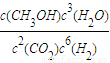 ;
;
 ;
; O2(g)=H2O(l)△H=-285.8kJ/mol;
O2(g)=H2O(l)△H=-285.8kJ/mol;

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
 (2012?湖南模拟)乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制得:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0
(2012?湖南模拟)乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制得:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0 乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取:
乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取: