
 (1)下列反应属于吸热反应的是DE
(1)下列反应属于吸热反应的是DE分析 (1)根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解反应以及某些复分解(如铵盐和强碱);
(2)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)①根据反应生成气体的快慢分析;根据阴阳离子判断;
②该反应是通过反应速率分析的,所以根据v=$\frac{△V}{△t}$判断.
解答 解:(1)A、葡萄糖被氧化放出大量的热,则属于放热反应,故A错误;
B、CH3COOH+和KOH反应放出大量的热,则属于放热反应,故B错误;
C、大多数化合反应放出热量,故C错误;
D、破坏生成物全部化学键所需能量小于破坏反应物全部化学键的能量,需要吸收能量,属于吸热反应,故D正确;
E、Ba(OH)2•8H2O晶体与NH4Cl晶体反应吸收热量,则属于吸热反应,故E正确;
F、金属与酸或水的反应放出热量,属于放热反应,故F错误;
故答案为:DE;
(2)A、随着反应的进行体系压强不变,容器内压强保持不变,不一定达平衡状态,故A错误;
B、混合气体的密度不变,说明气体的质量不变,即正逆反应速率相等,故B正确;
C、单位时间内生成n molC的同时生成n mol D,都是正反应方向,反应不一定达到化学平衡状态,故C错误;
D、反应体系中气体的物质的量是一定值,不一定平衡,故D错误;
E、A的物质的量不再变化,反应达到化学平衡状态,故E正确;
故答案为:BE;
(3)①该反应中产生气体,所以可根据生成气泡的快慢判断,氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用;硫酸钠和硫酸铜阴离子相同,可以消除阴离子不同对实验的干扰,
故答案为:反应产生气泡的快慢;控制阴离子相同,排除阴离子的干扰;
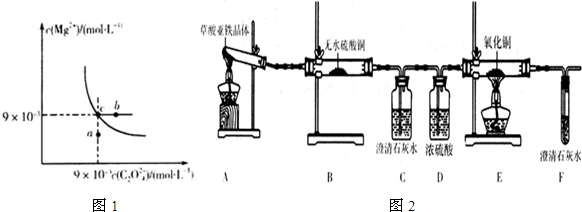
②由装置图可知,A是分液漏斗;该反应是通过生成气体的反应速率分析判断的,所以根据v=$\frac{△V}{△t}$判知,需要测量的数据是产生40ml气体所需要的时间;检查乙装置气密性的方法是:关闭A上的玻璃旋塞,将针筒的活塞拉出(或推进)一段后松开,活塞能回到原来的位置说明气密性良好;故答案为:分液漏斗;收集40mL气体所需要的时间;关闭A上的玻璃旋塞,将针筒的活塞拉出(或推进)一段后松开,活塞能回到原来的位置说明气密性良好.
点评 本题考查了吸热反应与放热反应的区别、化学平衡状态的标志、催化剂的作用及化学反应速率的影响因素等知识点,难度不大,要会分析将FeCl3改为Fe2(SO4)3更为合理的理由.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 由Zn和稀H2SO4反应制取氢气 | B. | 灼热的碳与二氧化碳反应 | ||
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合 | D. | 碳酸钙的分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol•L-1CH3COOH与0.1mol•L-1氨水等体积混合(PH=7):c(NH4+)=c(CH3COO-)=c(H+)=c(OH-) | |
| B. | 0.1mol•L-1HCl溶液与0.2mol•L-1氨水等体积混合(PH>7):c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-) | |
| C. | 0.1mol•L-1CH3COONa与0.1mol•L-1CaCl2溶液等体积混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 0.1mol•L-1Na2CO3溶液与0.1mol•L-1 NaHCO3溶液等体积混合:c(HCO3-)>0.05mol•L-1>c(CO32-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热氯化铁溶液,溶液颜色变深与盐类水解有关 | |
| B. | NaHS溶液水解方程式为:HS-+H2O?H2S+OH- | |
| C. | Na2SO3溶液中,c(OH-)=c(H+)+c(HSO3-)+c(H2SO3) | |
| D. | 0.1 mol•L-1的CH3COOH溶液和0.1 mol•L-1的CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 当闭合开关S1,断开开关S2,右石墨棒发生的电极反应为:2H2O-4e-=4H++O2↑ | |
| B. | 石墨棒使用前在高温火焰上灼烧至红热,迅速浸入冷水,可以使表面粗糙多空,吸附更多的气体 | |
| C. | 先闭合开关S1,一段时间后断开,再闭合S2,可以观察到发光二级管发光 | |
| D. | 断开S2,闭合S1,更换电解质,可以用来模拟工业制氯气,粗铜冶炼制精铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热使c(H+)增大 | B. | 投入一小块金属钠 | ||
| C. | 加入少量NH4Cl固体 | D. | 以铁为电极进行电解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电解质 | H2C2O4 | CH3COOH | HCN | H2CO3 |
| 电离常数(mol•L-1) | K1=5.6×10-2 K2=5.4×10-3 | K1=1.7×10-5 | K2=6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com