


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:不详 题型:单选题
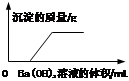
| A.肯定没有碳酸钠 |
| B.肯定有硫酸 |
| C.是否含有氯化铜不能确定 |
| D.至少含有硫酸或盐酸中的一种,也可能两种同时含有 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO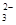 SO SO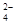 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3 | B.Na2CO3 | C.NaOH | D.Ca(OH) 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| | 错误观点 | 离子方程式 |
| ① | 所有的离子方程式均可以表示一类反应 | |
| ② | 所有酸碱中和反应均可表示为:H++OH-=H2O | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 阳离子 | Ag+、Mg2+、Al3+、Ba2+ |
| 阴离子 | Cl-、SO 、NO3-、OH- 、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.x=20时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>c(SO42-) |
| B.x=20时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+) |
| C.x=60时,溶液中有Ba2+、Al3+、OH-,且c(OH-) = c(Ba2+) |
| D.x=60时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应说明SO2有漂白性 |
| B.配平后H2O的计量系数为2(最简整数) |
| C.氧化剂与还原剂的物质的量之比为2:5 |
| D.每生成1mol Mn2+,共转移5 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com