
 nY(g) ��H=QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ������˵����ȷ����
nY(g) ��H=QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ������˵����ȷ����| �������/L c(Y)/mol/L �¶�/�� | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
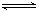 2NH3(g)��CO2(g) ��H =" a" kJ/mol
2NH3(g)��CO2(g) ��H =" a" kJ/mol | �¶�/�� | 15��0 | 20��0 | 25��0 | 30��0 | 35��0 |
| ƽ����ѹǿ/kPa | 5��7 | 8��3 | 12��0 | 17��1 | 24��0 |
| ƽ��������Ũ��/mol��L��1 | 2��4��10��3 | 3��4��10��3 | 4��8��10��3 | 6��8��10��3 | 9��4��10��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 pC�ﵽƽ�⣬����
pC�ﵽƽ�⣬�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC(g),��ƽ���C��ƽ�������е��������Ϊw����ά���¶Ȳ��䣬��1.2molA��0.4molB��0.6molCΪ��ʼ���ʣ���ƽ���ѹǿ���䣬C�����������Ϊw����x��ֵΪ
xC(g),��ƽ���C��ƽ�������е��������Ϊw����ά���¶Ȳ��䣬��1.2molA��0.4molB��0.6molCΪ��ʼ���ʣ���ƽ���ѹǿ���䣬C�����������Ϊw����x��ֵΪ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 C(g)��ƽ��ʱC ���������Ϊ40�G��
C(g)��ƽ��ʱC ���������Ϊ40�G���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Y(g)+Z(s)��������˵����Ӧ�ﵽƽ���־����( )
Y(g)+Z(s)��������˵����Ӧ�ﵽƽ���־����( )| A����������ѹǿ���ٱ仯 |
| B��X��Y��Z�����ʵ���֮��Ϊ2:1:1 |
| C����λʱ��������lmolY��ͬʱ�ֽ�2mol X |
| D��X�ķֽ�������Y������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4NO(g)+6H2O(g)��������������ȷ����
4NO(g)+6H2O(g)��������������ȷ����| A���ﵽ��ѧƽ��ʱ����ѧ��Ӧ���ʵĹ�ϵ��2v��(NH3)��3v�� (H2O) |
| B���ﵽ��ѧƽ��ʱ��NH3��O2��NO��H2O���ʵ���֮��Ϊ4��5��4��6 |
| C�����������ܶ�һ��ʱ���û�ѧ��Ӧ�ﵽ��ѧƽ�� |
| D������λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ�ﵽƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H2(g)+CO2(g)ƽ�ⳣ�����¶ȵı仯���±���
H2(g)+CO2(g)ƽ�ⳣ�����¶ȵı仯���±���| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
 H2(g)+CO2(g)������Ӧ��ƽ��ʱ��CO���������ΪX����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO���������������X����
H2(g)+CO2(g)������Ӧ��ƽ��ʱ��CO���������ΪX����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO���������������X���� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 ��һ���ؼ��IJ��衣
��һ���ؼ��IJ��衣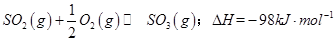 ����ʼʱ��100L���ܱ������м���4.0molSO2(g)��10.0molO2������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K=____________��
����ʼʱ��100L���ܱ������м���4.0molSO2(g)��10.0molO2������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K=____________��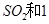 mol
mol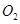 ,������Ӧ:
,������Ӧ: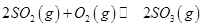 ,��ƽ���ı�����������
,��ƽ���ı�����������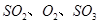 ����ƽ��Ũ�ȶ���ԭ���������____________(����ĸ)��
����ƽ��Ũ�ȶ���ԭ���������____________(����ĸ)��A�������¶Ⱥ�����������䣬����2mol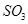 |
| B�������¶Ⱥ�����������䣬����2molN2 |
C�������¶Ⱥ�������ѹǿ���䣬����1mol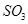 |
| D���ƶ�����ѹ������ |
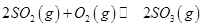 ��Ӧ��ͼ���У�����ȷ����_________��
��Ӧ��ͼ���У�����ȷ����_________��
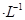 ��������Һ���������̹�ת����0.1mol����ʱ������������SO2�����Ϊ����״����Ϊ_________������Һ��pH="__________" (������Һ����仯)��
��������Һ���������̹�ת����0.1mol����ʱ������������SO2�����Ϊ����״����Ϊ_________������Һ��pH="__________" (������Һ����仯)�� �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com