
| A. | 火力发电厂的煤经粉碎、脱硫处理 | B. | 电镀废液经中和后直接排入到农田 | ||
| C. | 聚乳酸塑料代替传统塑料作购物袋 | D. | 回收并合理处理聚氯乙烯塑料废物 |
分析 A.煤经粉碎、脱硫处理,减少二氧化硫的排放;
B.电镀废液经中和后,可能含重金属离子;
C.聚乳酸塑料可降解,不会造成环境污染;
D.聚氯乙烯塑料难降解,污染环境.
解答 解:A.煤经粉碎、脱硫处理,减少二氧化硫的排放,利于环境保护,故A不选;
B.电镀废液经中和后,可能含重金属离子,则不能直接排入到农田,防止污染土壤,故B选;
C.聚乳酸塑料可降解,不会造成环境污染,则聚乳酸塑料代替传统塑料作购物袋,利用环境保护,故C不选;
D.聚氯乙烯塑料难降解,污染环境,则回收并合理处理聚氯乙烯塑料废物,利用环境保护,故D不选;
故选B.
点评 本题考查三废处理及环境保护,为高频考点,把握常见的环境污染物及污染物的处理为解答的关键,侧重分析与应用能力的考查,注意化学与环境的联系,题目难度不大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LSO3所含原子数为2NA | |
| B. | 标况下11.2LNO和11.2LO2混合后所得气体分子数为NA | |
| C. | 0.1mol•L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA | |
| D. | 1mol SiO2晶体中含有硅氧键的数目为4NA.而1mol金刚石中含碳碳键的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

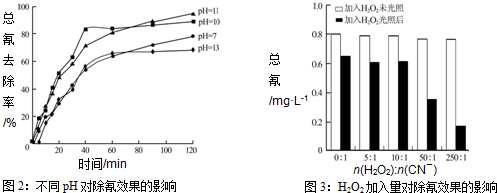
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1)K | ||||
| (2) | 18 | 20 | ||
| (3) | 16 | 18 | 32 |
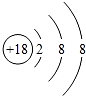 ,画出表中(3)的微粒结构示意图为
,画出表中(3)的微粒结构示意图为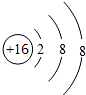 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 ,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物的化学式是SiO2.
,上述元素中,能和⑤号元素形成正四面体空间网状结构的化合物的化学式是SiO2.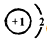 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com