
下列说法中,正确的是( )
A.氢键是一种化学键
B.氢键使物质具有较高的熔、沸点
C.能与水分子形成氢键的物质易溶于水
D.水结成冰体积膨胀与氢键无关
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol N2与足量的H2反应,转移的电子数是0.6NA
B.常温下,0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA
C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA
D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
 (1)该“84消毒液”的物质的量浓度约为____________ mol·L-1。
(1)该“84消毒液”的物质的量浓度约为____________ mol·L-1。
84消毒液,有效成分 NaClO
规格 1 000 mL
质量分数 25%
密度 1.19 g·cm-3
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=________ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是________(填序号)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
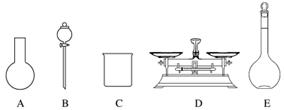
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1
②需用浓硫酸的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组分子之间存在氢键的是( )
①C2H6和CCl4 ②NH3和C6H6 ③CH3COOH和H2O ④CHCl3和CH2Cl2 ⑤HCHO和C2H5OH
A.①②④ B.③⑤
C.①②③④⑤ D.都不存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.化学键的极性越大,键就越强
B.凡能形成氢键的物质,其熔、沸点比同类物质的熔、沸点高
C.CFH3分子中,既有H原子,又有电负性大、半径小的F原子,因此,CFH3分子间可以形成氢键
D.稀有气体能在温度充分降低时液化,而且随相对分子质量的增大熔点升高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.冰融化时,分子中H—O键发生断裂
B.原子晶体中,共价键越强,熔点越高
C.分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
D.分子晶体中,分子间作用力越大,该物质越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期表中的位置如下图所示:

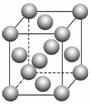
(1)写出F的基态原子核外电子排布式: 。E的晶胞结构如上图所示,该晶胞中含有金属原子的数目为________。
(2)C元素的第一电离能比同周期相邻的两种元素的第一电离能都高的原因是____________________________。
(3)由A、B、D三种元素形成的一种物质俗称光气,分子中A原子采取sp2杂化成键。光气分子的结构式是________,其中碳氧原子之间的共价键是________(填序号):
a.2个σ键
b.2个π键
c.1个σ键、1个π键
(4)
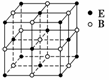
EB晶胞
EB晶胞如右图所示,EB晶体中E2+的配位数为____________,EB晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:EB-3 401 kJ·mol-1、NaCl-786 kJ·mol-1。导致两者晶格能差异的主要原因是____________________________________________。
(5)元素A形成的单质的晶体类型可以是原子晶体,如________(填写物质名称),也可以是________,如C60。
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是________(填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是__________(填化学式),反应的化学方程式为________________________________________________________________________。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有____(填字母)。
A.酸性 B.吸水性
C.脱水性 D.强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液____________,说明这种气体具有__________性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:_________________________。
(5)能否用澄清石灰水鉴别这两种气体?________(填“能”或“不能”),若不能,请填写两种能鉴别的试剂____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com