
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法不正确的是( )
)是其中的一种。下列关于该化合物的说法不正确的是( )
A. 与环庚烯互为同分异构体B. 二氯代物共有8种(不含立体异构)
C. 所有碳原子不可能处在同一平面D. 1mol该化合物含有18mol共价键
【答案】D
【解析】
A、该有机物的分子式为C7H12,与环庚烯的分子式相同,其结构不同,故互为同分异构体,故A不选;
B、![]() 有2种不同位置的H原子,若二氯代物中两个Cl原子位于同一个C原子上,有2种同分异构体,若位于不同C原子上,在一个四元环上,有2种不同位置;若位于两个四元环上,可能有4种不同结构,因此二氯代物共有2+2+4=8种,故B不选;
有2种不同位置的H原子,若二氯代物中两个Cl原子位于同一个C原子上,有2种同分异构体,若位于不同C原子上,在一个四元环上,有2种不同位置;若位于两个四元环上,可能有4种不同结构,因此二氯代物共有2+2+4=8种,故B不选;
C、在螺[3,3]庚烷(![]() )分子中的C原子都是饱和C原子,由于与C原子连接的原子构成的是四面体结构,最多有三个原子处于同一平面上,因此不可能所有碳原子处在同一平面上,故C不选;
)分子中的C原子都是饱和C原子,由于与C原子连接的原子构成的是四面体结构,最多有三个原子处于同一平面上,因此不可能所有碳原子处在同一平面上,故C不选;
螺[3,3]庚烷分子式是C7H12,1个分子中含有8个C—C键,含有12个C—H,所以一个分子中含有20个共价键,则1mol该化合物中含有20mol共价键,故D选;


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案科目:高中化学 来源: 题型:
【题目】有人尝试用工业制纯碱原理来制备![]() 。他向饱和
。他向饱和![]() 溶液中依次通入足量的______和______两种气体,充分反应后有白色晶体析出。将得到的白色晶体洗涤后灼烧,结果无任何固体残留,且产生的气体能使澄清石灰水变浑浊。写出生成白色晶体的化学方程式:________。分析该方法得不到
溶液中依次通入足量的______和______两种气体,充分反应后有白色晶体析出。将得到的白色晶体洗涤后灼烧,结果无任何固体残留,且产生的气体能使澄清石灰水变浑浊。写出生成白色晶体的化学方程式:________。分析该方法得不到![]() 的原因可能是_______________。
的原因可能是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法错误的是( )

A. 分子中含有三种含氧官能团
B. 既能与FeCl3发生显色反应,也能和Na2CO3反应
C. 既可以发生取代反应,又能发生加成反应
D. 1 mol该化合物最多能与6molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强.
⑴若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________L,V(H2)=________L.
⑵若剩余气体的体积为a L,则原CO和H2的混合气体中V(CO)∶V(H2)=________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一固定容积的密闭容器中进行反应:A2 +B2![]() 2AB。该条件下,A2、B2、AB均为气体。下列情况一定能说明该反应已达到化学平衡状态的是( )
2AB。该条件下,A2、B2、AB均为气体。下列情况一定能说明该反应已达到化学平衡状态的是( )
A. 气体的密度不再改变时
B. 气体的总物质的量不再改变时
C. 混合气体中各组分的含量不再改变时
D. 每消耗1molB2同时有2molAB生成时
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)下列反应属于放热反应的是_______。
A.铝片与稀H2SO4反应制取H2
B.碳酸钙高温分解成氧化钙和二氧化碳
C.葡萄糖在人体内氧化分解
D.氢氧化钾和硫酸中和
E.Ba(OH)2·8H2O与NH4Cl固体反应
(2)一定条件下,2L密闭容器中SO2与O2反应5min后,若SO2和SO3物质的量分别为0.1 mol和0.3mol,则SO2起始物质的量浓度为_____;用O2表示这段时间该化学反应速率为______。
(3)用活性炭还原法处理氮氧化物。有关反应为C(s)+2NO(g)![]() N2(g)+CO2(g),某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,下列说法不能作为判断该反应达到化学平衡状态标志的是________(填选项字母)
N2(g)+CO2(g),某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,下列说法不能作为判断该反应达到化学平衡状态标志的是________(填选项字母)
A.活性炭的质量保持不变 B.v正(N2)=2v逆(NO)
C.容器内气体压强保持不变 D.容器内混合气体的密度保持不变
E.容器内混合气体的平均相对分子质量保持不变 F.容器内CO2的浓度保持不变
(4)利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能利用化学能,装置如图所示:
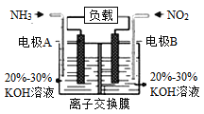
①A电极的电极反应式为_______________。
②下列关于该电池的说法正确的是___________(填选项字母)。
A.电子从右侧电极经过负载后流向左侧电极
B.离子交换膜为阴离子交换膜,则OH-由右侧溶液移向左侧溶液
C. 当有4.48L NO2被处理时,转移电子的物质的量为0.8mol
(5)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。已知: 1molN2和3molH2反应生成2molNH3时放出热量93kJ,试根据表中所列键能数据计算a的数值_________。
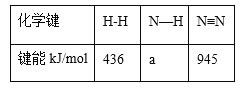
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。


(1)已知该实验反应的反应方程式为:__Fe+__H2O![]() __Fe3O4+__H2(请配平)。
__Fe3O4+__H2(请配平)。
(2)仪器a的名称是___。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃__(填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用图中__(填“甲”“乙”或“丙”)装置。
②称取5.6g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448L,则铁粉的转化率为___。(转化率=![]() )
)
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:
步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
Ⅰ.取样,滴加KSCN溶液 | 溶液不变红色 | ①Fe3O4+8H+=Fe2++2Fe3++4H2O ②___ | Ⅲ.反应后的溶液中阳离子___ |
Ⅱ.取样,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现白色沉淀,迅速变为灰绿色,最终变为___色 | ①___ ②Fe2++2OH—=Fe(OH)2↓ ③4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化一定浓度的FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测不合理的是( )
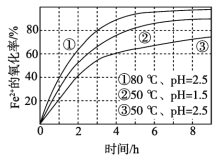
A.Fe2+的氧化率随时间延长而逐渐增大
B.由①和③可知,温度越高,Fe2+氧化速率越快
C.由②和③可知,pH越大,Fe2+氧化速率越快
D.氧化过程的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中:互为同分异构体的是___,互为同系物的是__,属于同一种物质的是___。
A.CH3CH2CH3、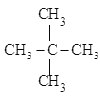 B.CH3-CH=CH-CH3、CH2=CH-CH2-CH3 C.CH2=CH-CH3、C2H4 D.
B.CH3-CH=CH-CH3、CH2=CH-CH2-CH3 C.CH2=CH-CH3、C2H4 D.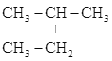 、
、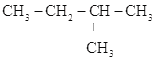 E.CH3CH2CH2COOH、CH3COOCH2CH3
E.CH3CH2CH2COOH、CH3COOCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com