
| 1 |
| 2 |
| 3 |
| 2 |

| 1 |
| 2 |
| 3 |
| 2 |
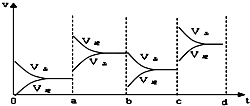 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
| A、H2SO3 的摩尔质量是82g |
| B、1molH2O的质量是 18 g/mol |
| C、Cl- 的摩尔质量是35.5 g/mol |
| D、1molN2 的体积是 22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、③④ | C、②⑤ | D、①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②④⑤ |
| C、①③⑥ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
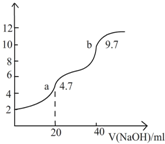 用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示.下列有关说法错误的是( )
用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示.下列有关说法错误的是( )| A、H2A的物质的量浓度为0.1000mol.L-1 |
| B、H2A是二元弱酸 |
| C、a-b段发生反应HA-+OH-=H2O+A2- |
| D、a点时HA-的水解程度大于电解程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com