
有一反应:2A+B 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,图中有a、b、c三点,如图所示,则下列描述正确的是
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,图中有a、b、c三点,如图所示,则下列描述正确的是
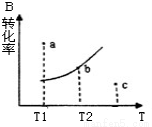
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下a点表示若想达到平衡,可以采取增大压强的方法
D.c点可表示v(正)<v(逆)
科目:高中化学 来源:2016-2017学年云南省高一上期中化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列说法正确的是( )
A.将1 L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA
B.1 L 0.1 mol/L NaHSO4溶液中含有0.1 NA个HSO4-
C.常温常压下,23 g NO2和N2O4的混合气体一定 含有NA个氧原子
含有NA个氧原子
D.1 mol铁与足量稀盐酸反应转移的电子数目为3NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:选择题
由1-溴丁烷制取少量的1,2-丁二醇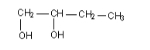 时,需要经过下列哪几步反应
时,需要经过下列哪几步反应
 A.取代、消去、加成 B.加成、消去、取代
A.取代、消去、加成 B.加成、消去、取代
 C.消去、加成、取代 D.消去、加成、消去
C.消去、加成、取代 D.消去、加成、消去
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
向三份0.1 mol·L-1NH4Cl溶液中分别加入少量Mg、NaOH、FeSO4固体(忽略溶液体积变化),则溶液中NH4+浓度的变化依次为
A.减小、增大、减小 B.减小、增大、增大
C.增大、减小、减小 D.减小、减小、增大[]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
现有常温下四份等体积的酸或碱溶液:①0.01 mol/L CH3COOH;②0.01 mol/L HCl;③pH=12的氨水;④pH=12的NaOH溶液。以下有关说法正确的是
A.将四份溶液稀释相同倍数后,溶液的pH:③>④>①>②
B.将①、④等体积混合,则混合液的pH为7
C.四份溶液中水的电离程度由大到小的顺序为:③>①=②=④
D.将②加入③至恰好完全反应,则消耗体积为③>②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ /mol;HCl(aq)与NaOH(aq)反应的△H =-55.6kJ/ mol。则HCN在水溶液中电离的ΔH等于
A.-67.7 kJ /mol B.-43.5kJ /mol C.+43.5 kJ/ mol D.+67.7 kJ/ mol
B.-43.5kJ /mol C.+43.5 kJ/ mol D.+67.7 kJ/ mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:推断题
已知某有机物的相对分子质量为58,请回答:
(1)若该有机物为烃,且含有支链,则其名称为________________________。
(2)若为结构中只含1个-CH3和一个官能团的含氧衍生物,则官能团的名称为 。
(3)若为结构中有2个 — CH3含氧衍生物,则可能的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:选择题
下列各组中的反应,属于同一反应类型的 是( )
是( )
A.溴丙烷和氢氧化钠溶液反应制丙醇;丙烯与水反应制丙醇
B.甲苯硝化制对硝基甲苯;甲苯和高锰酸钾反应制苯甲酸
C.1—氯环己烷制环己烯;丙烯与溴反应制1,2—二溴丙烷
D.苯甲酸乙酯水解制苯甲酸和乙醇;乙酸和乙醇制乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:填空题
氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
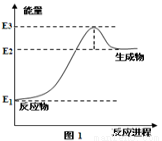
(2)以甲烷为原料可制得氢气。图1是一定温度、压强下,CH4(g)与H2O(g)反应生成CO(g)和1mol H2(g)的能量(KJ)变化示意图,写出该反应的热化学方程式_______________(△H用E1、E2、E3表示)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g) MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
A.容器内气体压强保持不变
B.吸收y mol H2只需1 mol MHx
C. 若降温,该反应的平衡常数
若降温,该反应的平衡常数 增大
增大
D.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH- FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。

①电解一段时间后,c(OH-)降低的区域在__________(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_____________。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c(  Na2FeO4)低于最高值的原因:_____________。
Na2FeO4)低于最高值的原因:_____________。
(5)在容积可变的密闭容器中充入10molCO和20molH2,发生CO ( g ) + 2H2 ( g ) CH3OH ( g ) △H<0, CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为1 L。若反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)= L。
CH3OH ( g ) △H<0, CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为1 L。若反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)= L。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com