
【题目】Ⅰ.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X、Y既不同族,也不同周期。X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价
的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)请写出M的元素符号:____________,Z的原子结构示意图:_____________。M与X两元素可形成两种液态化合物,其化学式分别为________________________。
(2)请写出N元素在周期表中的位置:___________________________;与N同族的短周期元素L,其最高价氧化物的电子式为_______________________。
(3)Y与Z相比,非金属性较强的元素是__________(填元素符号),可以证明该结论的实验事实是_________________________________________________________________。
Ⅱ.下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。
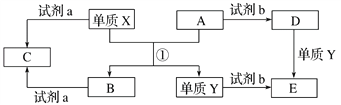
(1)请写出反应①的化学方程式:_____________________________________。
(2)由D到E的离子方程式:__________________。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:__________________________________________________________________。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是______________________________。
【答案】 H ![]() H2O、H2O2 第3周期ⅣA族
H2O、H2O2 第3周期ⅣA族 ![]() Cl Cl2+H2S===S↓+2HCl(其他答案合理也可) Fe2O3+2Al
Cl Cl2+H2S===S↓+2HCl(其他答案合理也可) Fe2O3+2Al![]() 2Fe+Al2O3 Fe+2Fe3+===3Fe2+ 2Al+2OH-+2H2O===2AlO
2Fe+Al2O3 Fe+2Fe3+===3Fe2+ 2Al+2OH-+2H2O===2AlO![]() +3H2↑ 2FeSO4+H2SO4+2NaNO2===2Fe(OH)SO4+Na2SO4+2NO↑
+3H2↑ 2FeSO4+H2SO4+2NaNO2===2Fe(OH)SO4+Na2SO4+2NO↑
【解析】Ⅰ.X、Y、Z、M、N为短周期的五种主族元素,X原子最外层电子层数是核外电子层数的三倍,X是氧元素,X、Z同族,Z是硫元素;Y、Z同周期,Y最高化合价与其最低化合价的代数和为6,Y是氯元素;N是最短周期主族元素中原子半径最大的非金属元素,N是硅元素;M与X、Y即不同族,也不同周期,M是氢元素。
(1)氢的元素符号是:H;硫的原子结构示意图是:![]() ;氢与氧两元素可形成两种液态化合物,其化学式分别为:H2O、H2O2。
;氢与氧两元素可形成两种液态化合物,其化学式分别为:H2O、H2O2。
(2)硅元素在周期表中的位置是:第3周期ⅣA族;与硅同族的短周期元素是碳,其最高价氧化物的电子式为:![]() 。
。
(3)氯与硫相比,非金属性较强的元素符号是:Cl,可以证明该结论的实验事实是:Cl2+H2S=S↓+2HCl。
Ⅱ.根据题意A为Fe2O3,X为铝,通过铝热反应生成氧化铝(B)和铁(单质Y);D与Fe反应生成E,则试剂b为盐酸,D、E分别是铁盐和亚铁盐。
(1)反应①所表示的铝热反应的化学方程式为:Fe2O3+2Al![]() 2Fe+Al2O3。
2Fe+Al2O3。
(2)由Fe3+到Fe2+的离子方程式为:Fe+2Fe3+=3Fe2+。
(3)铝与氢氧化钠溶液反应的离子方程式是:2Al+2OH-+2H2O=2AlO2- +3H2↑
(4)E为FeSO4(铁的化合价为+2价)→Fe(OH)SO4(铁的化合价为+3价),而NaNO2(氮的化合价为+3价)→NO(氮的化合价为+2价)。根据电子得失守恒、质量守恒定律即可配平反应化学方程式得:2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑。


科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅰ]支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是
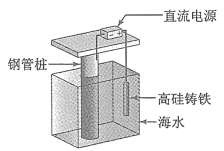
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以I—的形式存在。实验室里从海带中提取碘的流程如下:(已知C12+2KI=2KCl+I2)
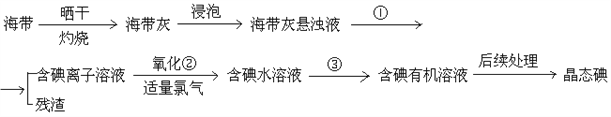
(1)步骤①的操作方法是________;除漏斗、烧杯外,还需要使用的玻璃仪器是__________。
(2)提取碘的过程中,可供选择的萃取剂是(______)
A、苯、酒精 B、CCl4、苯 C、汽油、醋酸
(3)步骤③的操作中,所用的主要玻璃仪器是_________________。当将含碘有机溶液静置分层后,若要取出下层液体的接下来的操作是:________________________________________
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏过程,蒸馏实验中用到的主要玻璃仪器有:温度计、牛角管、酒精灯、____________、__________、锥形瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
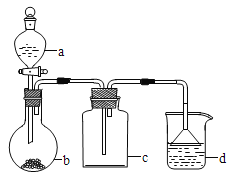
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:
A.烧碱 B.硫酸 C.干冰 D.硫酸钡 E.纯碱 F.铁
(1)既不是电解质,也不是非电解质的是 。
(2)纯碱的电离方程式是 。
(3)烧碱溶液与稀硫酸混合,发生反应的离子方程式为______________________________。
(4)将干冰升华后所得的气体通入过量烧碱溶液中,发生反应的离子方程式为 。
(5)a、b、c、d分别是Na2CO3、BaCl2、HCl、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
反应物 | a+b | c+d | a+d | a+c | b+d |
现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
①b是 (用化学式填写)。
②写出a+c反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的原子最外层有2个电子,该元素( )
A. 一定是金属元素 B. 最高化合价一定为+2价
C. 一定是ⅡA族元素或是He D. 无法确定属于哪类元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关微粒性质的比较中不正确的是
A. 离子半径:O2->Na+>Mg2+ B. 原子的未成对电子数:Mn>Ge>Br
C. 元素的第一电离能:O>N>C D. 元素的电负性:F>N>Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 同一原子中, ls、2s、3s电子的能量逐渐增多
B. 同一原子中,2p、3p、4p能级的轨道数依次增多
C. 任一原子的p能级电子云轮廓图形状均呈哑铃形
D. 任一能层的能级数等于该能层序数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向足量的500 mL NaOH溶液中投入10.8 g Al,二者恰好完全反应。试计算:
(1)Al的物质的量。
(2)参加反应的NaOH的物质的量和溶液的物质的量浓度。
(3)生成标准状况下H2的体积。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com