
���� ��1����̪�����죬����NaOH����ķ�Ӧ���������������������
��2�����ü����μӼ�ķ��������ʵ�飬����ɫ�ָ�˵������к�ʹ����٣�����ɫ���ָ�����˵���Ǵ���������ã�
��� �⣺��1�����̪�����죬��������ˮ�������뺬��̪��NaOHϡ��Һ�У����ε����һ��ʱ��ɫͻȻ��ȥ��������У�����ˮ�еĴ�������Ư���ԣ�ʹ��Һ�ɺ�ɫ�����ɫ������ˮ��NaOH��Ӧ�������Ȼ��ơ��������ƣ���Һ���Լ�������Һ�����ɫ��
�ʴ�Ϊ����ˮ�е��������к��������ƣ�ʹ��Һ�ɺ�ɫ�����ɫ��
��2���������Ư�����Һ�ټ�NaOH��Һ����ָ���ɫ�����������Һ�еμ�NaOH��Һ������Һ��Ϊ��ɫ��˵������ȷ������Һ�ָ���ɫ��˵������ȷ��
�ʴ�Ϊ����Ϊ��ɫ���ָ���ɫ��
���� ���⿼����ˮ��������ʼ��������Ư���ԣ���Ŀ�ѶȲ�����ȷ������̪��켰��ˮ�ijɷ֡����ɷֵ������ǽ����Ĺؼ�������������ѧ�����Ӧ����ѧ֪ʶ��������


 �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д� һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д� ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ö����ЧӦ����FeCl3��Һ��Fe��OH��3���� | |
| B�� | ��KOH��Һ����NH4Cl��AlCl3��MgSO4��FeCl3������Һ | |
| C�� | ��������Һ����Na2CO3��Һ��Na2SiO3��Һ | |
| D�� | ��BaCl2��Һ����AgNO3��Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԭ�ӽṹʾ��ͼ��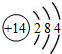 | B�� | ��ϩ���ӱ���ģ�ͣ�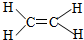 | ||
| C�� | ��������ӵĵ���ʽ��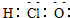 | D�� | ������ӵĽṹ��ʽ��C2H4O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��6 | B�� | 2��15 | C�� | 2��11 | D�� | 1��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m=4 R2+�ǻ�ԭ�� | B�� | m=n R3+���������� | ||
| C�� | m=2 R2+�������� | D�� | m=y R3+�ǻ�ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4 L N2��NH3���������ԭ�Ӽ乲��3NA�����õ��Ӷ� | |
| B�� | 3.0 g��ȩHCHO�����������й���̼ԭ����Ϊ0.1NA | |
| C�� | 25��ʱpH=1�Ĵ�����Һ�к���H+����ĿΪ0.1NA | |
| D�� | ��״���£�2.24 L CH2Cl2���еķ�����Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������Cl2 | |
| B�� | �������뻹ԭ�������ʵ���֮��Ϊ3��8 | |
| C�� | ÿ����1molN2��ת��3mol���� | |
| D�� | ��������δ��������NH3���ʵ���֮��Ϊ1��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
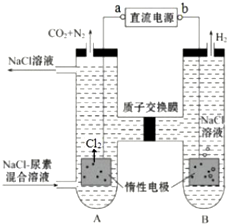 ���ڹ�����ռ����Ҫ��λ�����й㷺����;��
���ڹ�����ռ����Ҫ��λ�����й㷺����;��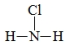 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com