
| A. |  1,3,4-三甲苯 1,3,4-三甲苯 | |
| B. |  3-乙基-1-丁烯 3-乙基-1-丁烯 | |
| C. | 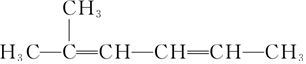 2-甲基-2,4-己二烯 2-甲基-2,4-己二烯 | |
| D. |  2,4,4-三甲基戊烷 2,4,4-三甲基戊烷 |
分析 判断有机物的命名是否正确或对有机物进行命名,其核心是准确理解命名规范:
(1)烷烃命名原则:
①长:选最长碳链为主链;
②多:遇等长碳链时,支链最多为主链;
③近:离支链最近一端编号;
④小:支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简:两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:A. ,苯环上取代基位次和应最小,正确名称为:1,2,4-三甲苯,故A错误;
,苯环上取代基位次和应最小,正确名称为:1,2,4-三甲苯,故A错误;
B. 为烯烃,选取含碳碳双键在内的最长碳链为主碳链,含5个碳,离双键近的一端编号得到名称3-甲基-1-戊烯,故B错误;
为烯烃,选取含碳碳双键在内的最长碳链为主碳链,含5个碳,离双键近的一端编号得到名称3-甲基-1-戊烯,故B错误;
C.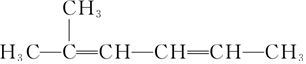 为二烯烃,选取含两个碳碳双键在内的最长碳链为主碳链,含6个碳,离双键近的一端编号且取代基位次和最小,得到名称 2-甲基-2,4-己二烯,故C正确;
为二烯烃,选取含两个碳碳双键在内的最长碳链为主碳链,含6个碳,离双键近的一端编号且取代基位次和最小,得到名称 2-甲基-2,4-己二烯,故C正确;
D. 为烷烃,选取最长碳链含5个碳,离取代基近的一端编号得到名称2,2,4-三甲基戊烷,故D错误;
为烷烃,选取最长碳链含5个碳,离取代基近的一端编号得到名称2,2,4-三甲基戊烷,故D错误;
故选C.
点评 本题考查了有机物的命名,题目难度中等,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 合成高分子的小分子就是高分子的链节 | |
| B. | 缩聚反应的产物只有高分子 | |
| C. | 聚乙烯具有热塑性 | |
| D. | 1mol 水解后只能与1molNaOH反应 水解后只能与1molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 单质的还原性:Y>X | |
| B. | 元素M与N能形成的共价化合物不止一种 | |
| C. | 通常状况下,元素Z的单质不能与元素M的氧化物反应 | |
| D. | 元素X、Y、Z的最高价氧化物对应的水化物彼此间均可发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2有漂白性,可广泛用于食品增白工业 | |
| B. | 浓硫酸不能与Al反应,故可用铝槽车运送浓硫酸 | |
| C. | 14C可用于文物年代鉴定,14C与12C互为同位素 | |
| D. | 从海水中提取的所有物质都须通过化学反应才能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 )中标有“*’’的碳原子即为手性碳原子.
)中标有“*’’的碳原子即为手性碳原子. 或
或 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等.
已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com