
����Ŀ���Ի�ͭ����Ҫ�ɷ���CuFeS2������������SiO2��Ϊԭ����ͭ�ķ����в�ͬ��ұ������������ͭ������ͭ��Cu2S���ڿ����и��±��ռ��ɵõ�ͭ��һ�ֻ�ԭ�Ե����塣��������ʪ����ͭ�����½�չ����ѧ�ҷ�����һ��ϸ��������ˮ��Һ�����������£����Խ���ͭ�������������Ρ�ij�������ø�ԭ������ͭ���̷���FeSO47H2O���Ĺ������£�
�ش��������⣺
��1������ͭ�����Ļ�ѧ����ʽ��_________________________��
��2��ʪ����ͭ���������У�Ϊ��������ʱ�Ľ�ȡ�ʣ������̿ɲ�ȡ�Ĵ�ʩ��________���Լ�XΪ__________����������_____________��
��3���Լ�aΪ______________���Լ�bΪ______________��
��4����ƽ��Ӧ1�Ļ�ѧ����ʽ��____CuFeS2+___H2SO4+____O2=____CuSO4+____Fe2��SO4��3+____H2O
��5����֪��������Ksp[Cu��OH��2]=2.2��10-20��Ksp[Fe��OH��3]=2.6��10-39������������Լ�X����pH=4ʱ����ʹ��Һ�е�Fe3+ת��ΪFe��OH��3����������Һ�е�c��Fe3+��=___________����Ҫ��ʱ������Cu��OH��2����������Һ�е�Cu2+Ũ�������_________________��
���𰸡���1��Cu2S+O2![]() 2Cu+SO2��2�֣� ��2�����裨�������������۴��������ܵ÷֣���1�֣� CuO��CuCO3��Cu��OH��2��1�֣� ����pH��ʹ�����ӳ�������2�֣���3��H2SO4��1�֣���Fe��1�֣�(4) 4��2��17��4��2��2��2�֣� (5)2.6��10-9 mol/L��2�֣�;2.2mol/L��2�֣�
2Cu+SO2��2�֣� ��2�����裨�������������۴��������ܵ÷֣���1�֣� CuO��CuCO3��Cu��OH��2��1�֣� ����pH��ʹ�����ӳ�������2�֣���3��H2SO4��1�֣���Fe��1�֣�(4) 4��2��17��4��2��2��2�֣� (5)2.6��10-9 mol/L��2�֣�;2.2mol/L��2�֣�
��������
�����������1������ͭ��ԭ���ǽ���ͭ��Cu2S���ڿ����и��±��ռ��ɵõ�ͭ��һ�ֻ�ԭ�Ե����壬�������Ƕ���������˷�Ӧ�ķ���ʽΪCu2S+O2![]() 2Cu+SO2��
2Cu+SO2��
��2�����������¶Ȼ��ƻ������ʣ����Ϊ��������ʱ�Ľ�ȡ�ʣ������̿ɲ�ȡ�Ĵ�ʩ�ǽ��裻���ڲ������������ʣ������ٵ�����Һ��pHֵ����������ʱӦ��ѡ������ͭ������������̼��ͭ�ȡ�
��3�����ڼ�������ͭ������Һ��pH�����������������������ʹ���A�� Fe��OH��3��Ҫ�Ʊ��̷�������Ҫ����ϡ���ᣬ�õ���������Ȼ���ټ������۵õ������������ɣ���a�����ᣬb������
��4�����ݷ���ʽ��֪��Ԫ�صĻ��ϼ۴���2�����ߵ���3�ۣ�ʧȥ1�����ӣ�SԪ�صĻ��ϼ۴ӣ�2�����ߵ���6�ۣ�ʧȥ8�����ӣ���1mol CuFeS2ʧȥ17mol���ӣ�1mol�����õ�4mol���ӣ���˸��ݵ��ӵ�ʧ�غ��֪��Ӧ�ķ���ʽΪ4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2��SO4��3+2H2O��
��2��pH��4ʱ��Һ��������Ũ����10��10mol/L������������������ܶȻ�������֪��Һ��c��Fe3+����![]() ��2.6��10-9 mol/L������������ͭ���ܶȻ�������֪��ʱ��Һ��ͭ����Ũ�ȣ�
��2.6��10-9 mol/L������������ͭ���ܶȻ�������֪��ʱ��Һ��ͭ����Ũ�ȣ�![]() ��2.2mol/L�������Ҫ��ʱ������Cu��OH��2����������Һ�е�Cu2+Ũ�������2.2mol/L��
��2.2mol/L�������Ҫ��ʱ������Cu��OH��2����������Һ�е�Cu2+Ũ�������2.2mol/L��


 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH2 = CH��CH2OH�����ʿ����У��� �ӳɷ�Ӧ ��������Ӧ�� ������Ӧ �� �кͷ�Ӧ
A��ֻ�Т٢� B��ֻ�Т٢ڢ� C��ֻ�Т٢ۢ� D��ֻ�Т٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����S2Cl2���ǹ㷺������ҵ��������������һ�ֳȻ�ɫ�ж����Һ�壬���ķ��ӽṹ��ͼ��ʾ��

��1��S2Cl2�ĽṹʽΪ ���仯ѧ�������� ������Լ������Ǽ��Լ������Լ��ͷǼ��Լ�������
��2���縺�ԣ�S ���������������Cl��S2Cl2����Ļ��ϼ�Ϊ ��
��3��S2Cl2������Sԭ�ӵ��ӻ��������Ϊ ��ÿ��Sԭ���� �Ի����Ӷԣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
(1)�����£�����������������ʢװŨ�����ԭ���� ��
(2)����������������װNaOH�ȼ���Һ��ԭ����(�����ӷ���ʽ��ʾ) ��
(3)��ҵ��ұ��������Ӧ�Ļ�ѧ����ʽΪ ��
(4)ijʵ��С��������ͼװ����֤����ˮ�����ķ�Ӧ��
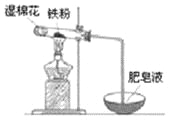
��ʪ���������� ���Թ��з�Ӧ�Ļ�ѧ����ʽ�� ��
��ʵ�������ȡ��������Ӧ��Ĺ������Թ��У�����������ᣬ������ȫ�ܽ⣬������Һ�д��ڵ��������� (�����)��
a��һ����Fe2+��H+��Fe3+b��һ����Fe2+��H+��������Fe3+
c��һ����Fe2+��Fe3+��������H+d��һ����Fe3+��H+��������Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ΰ������ĸ���Һ�䷴Ӧ��Сʵ�飬���Ӧ��Ӧ�����ӷ���ʽ��д��ȷ���ǣ� ��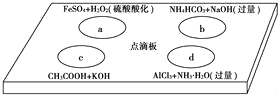
A��a��Ӧ��Fe2++2H++H2O2�TFe3++2H2O
B��b��Ӧ��HCO3��+OH���TCO32��+H2O
C��c��Ӧ��H++OH���TH2O
D��d��Ӧ��Al3++3NH3H2O�TAl��OH��3��+3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ��ͨ����ѧ��Ӧ��������( )
A. ̫����
B. ��ϫ��
C. ����
D. ����ȼ�ղ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����м���ʵ���У���ѡ�Լ�����������( )
A����ˮ�����Ҵ��ͱ�
B����̼��������Һ����������Ҵ�
C�������Ƶ�������ͭ���������Ǻ�����
D���ø������������Һ����ױ��ͼ�ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=2������һԪ��x��y�������Ϊ100ml��ϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ���ֱ�μ�NaOH��Һ��c=0.1mol/L����pH=7������NaOH��Һ�����ΪVx��Vy����

A��xΪ����Vx��Vy B��xΪǿ��Vx��Vy C��yΪǿ��Vx��Vy D��yΪ����Vx��Vy
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A������ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2��
B��Cu�ӵ�ϡ�����У�Cu+2H+�TCu2++H2��
C��������NaOH��Һ��Ӧ��Cl2+OH-�TCl-+ClO-+H2O
D��̼����������Һ��Ӧ��CaCO3+2H+�TCa2+ +CO2��+H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com