
| A.NaHCO3=Na++HCO3- | B.NaHSO4═Na++H++SO42- |
| C.H2SO4═2H++SO42- | D.KClO3═K++Cl-+3O2- |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
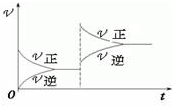
| A.正反应是吸热反应,m+n<p+q |
| B.逆反应是吸热反应,m+n<p+q |
| C.正反应是吸热反应,m+n>p+q |
| D.逆反应是吸热反应,m+n>p+q |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 催化剂 |
| △ |
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2CO3?2H++CO32- | B.HClO═H++ClO- |
| C.NaHCO3?Na++HCO3- | D.Ba(OH)2═Ba2++2OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K2CO3═2K++CO32- | B.KClO3═K++Cl-+3O2- |
| C.NaOH═Na++OH- | D.NaHCO3═Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-) | B.pH | C.c(NH4+)/c(NH3·H2O) | D.c(H+)·c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
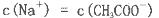
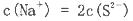
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
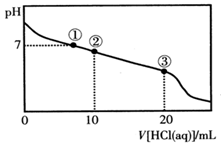
| A.点①所示溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-) |
| B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) |
| C.点③所示溶液中:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) |
| D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com