
2013年12月12日,中国矿业报报道中国地质科学院矿产综合利用研究所认定石龙铜矿含铜品位高(含铜3.27%)。已知铜矿物以黄铜矿、斑铜矿和辉铜矿为主。黄铜矿(CuFeS2)既是制取铜及其化合物的主要原料,又可以制备硫及铁的化合物。请回答下列问题:
(1)冶炼铜的反应方程式为8CuFeS2+21O2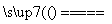 8Cu+4FeO+2Fe2O3+16SO2↑,若CuFeS2中铁元素为+2价,则反应中被还原的元素为________(填元素名称)。
8Cu+4FeO+2Fe2O3+16SO2↑,若CuFeS2中铁元素为+2价,则反应中被还原的元素为________(填元素名称)。
(2)上述冶炼过程中产生大量二氧化硫,下列对其性质的描述中正确的是________(填序号)。
A.SO2既是氧化剂,又是还原剂
B.SO2是还原产物
C.SO2是形成酸雨的一种物质
D.SO2是氧化产物
(3)SO2的存在对CO2的检验会造成干扰,实验室常用酸性高锰酸钾溶液除去SO2,请写出该反应的化学方程式:
_______________________________________________________________。
(4)利用黄铜矿冶炼产生的炉渣(含FeO、Fe2O3、SiO2、Al2O3)可制备Fe2O3。方法为先用稀盐酸浸取炉渣,过滤;将滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。用下列哪些试剂可以验证炉渣中含有FeO?________________(填序号)。其中发生氧化还原反应的离子方程式为____________________。
A.稀盐酸 B.稀硫酸 C.KSCN溶液
D.KMnO4溶液 E.NaOH溶液 F.碘水
解析 该题以黄铜矿为载体,考查了氧化还原反应的相关概念、氧化还原反应方程式的书写以及亚铁离子的检验。(1)要找出反应中被氧化或被还原的元素,突破口是化合价的升降。由于+2价的铁部分升高为+3价,因而铁元素被氧化,同时硫元素由-2价升高为+4价,所以硫元素也被氧化。由氧元素的化合价变化情况可知氧气在反应中作氧化剂,同时铜元素由+2价降低为0价,所以铜元素被还原。(2)SO2既是O2被还原的产物,又是CuFeS2被氧化的产物,还是形成酸雨的一种大气污染物。(3)SO2具有还原性,KMnO4具有强氧化性,在酸性条件下,KMnO4被还原为MnSO4,SO2被氧化成硫酸,所以反应的化学方程式为5SO2+2KMnO4+2H2O===K2SO4+2MnSO4+2H2SO4。(4)要验证炉渣中有FeO,若用常规方法,很难实现。因为炉渣中存在Fe2O3,酸溶后,溶液中既有Fe2+,又有Fe3+,而Fe3+干扰Fe2+的检验。此时就要考虑FeO的另一个性质,即FeO的还原性,用强氧化剂将其氧化,若反应过程中有明显的现象变化,就能达到目的。根据题目提供的试剂可选择稀硫酸和KMnO4溶液。其中发生氧化还原反应的离子方程式为5Fe2++MnO +8H+===5Fe3++Mn2++4H2O。
+8H+===5Fe3++Mn2++4H2O。
答案 (1)铜元素、氧元素 (2)BCD (3)5SO2+2KMnO4+2H2O===K2SO4+2MnSO4+2H2SO4 (4)BD 5Fe2++MnO +8H+===5Fe3++Mn2++4H2O
+8H+===5Fe3++Mn2++4H2O


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列鉴别苯与己烯的实验方法与判断都正确的是( )
|
| A. | 分别加入溴水振荡,上下两层颜色都消失的是己烯 |
|
| B. | 分别加入溴水振荡,下层颜色消失的是己烯 |
|
| C. | 分别点燃,无黑烟生成的是苯 |
|
| D. | 分别加入酸性KMnO4溶液振荡,静置后有机层为无色的是己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于原子结构及微粒间的数量关系的说法不正确的是(双选)( )
A.同种元素的原子均有相同的质子数和中子数
B.微粒+、Mg2+、O2-具有相同的电子层结构
C.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
D.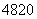 Ca2+的中子数比核外电子数多8
Ca2+的中子数比核外电子数多8
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表短周期的一部分,下列说法中正确的是( )
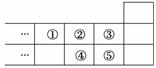
A.元素①位于第二周期第ⅣA族
B.气态氢化物的稳定性:④>②
C.最高价氧化物对应水化物的酸性:⑤>④
D.元素的最高正化合价:③=⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:_____________________________________________。
(2)[2013·广东理综,32(3)]完成煅烧过程中一个反应的化学方程式:________CuO+________Al2O3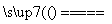 ________CuAlO2+________↑。
________CuAlO2+________↑。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有0.005 mol FeBr2及其他物质,向该溶液中通入134.4 mL标准状况下的Cl2,溶液中只有FeBr2与Cl2反应,则通入Cl2后溶液中可能大量存在的离子是( )
A.Fe2+、Fe3+、Br-、NO B.Fe2+、H+、NO
B.Fe2+、H+、NO 、K+
、K+
C.Fe3+、Br-、NO 、Cl- D.Fe2+、Br-、NO
、Cl- D.Fe2+、Br-、NO 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO 、SO
、SO 、Cl-、I-、HCO
、Cl-、I-、HCO ,取该溶液进行如下实验:
,取该溶液进行如下实验:
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴甲基橙溶液 | 溶液变红色 |
| ②取少量该溶液,加入铜片和浓硫酸,加热 | 有无色气体产生,遇空气可以变成红棕色 |
| ③取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断:
(1)溶液中一定存在的离子是________;溶液中肯定不存在的离子是____________________________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称(若为溶液反应,说明使用试剂的名称,不必写详细步骤)_________________________ _______________________________________________。
(3)写出实验⑤中所有反应的离子方程式: ________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数的值为NA,下列叙述正确的是( )
A.在铜与硫的反应中,1 mol铜参加反应失去的电子数为2NA
B.常温下,32 g含有少量臭氧的氧气中,含有的氧原子数为2NA
C.若1 mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA
D.78 g过氧化钠固体中所含阴、阳离子总数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应2SO2(g)+O2 (g) 2SO3(g),下列判断中正确的是( )
2SO3(g),下列判断中正确的是( )
A.2体积SO2和足量O2反应,生成 2体积SO3
B.恒温恒容,通入气体氦使压强增大,平衡向右移动
C.平衡时,SO2消耗速率等于O2生成速率的两倍
D.平衡时,SO2浓度等于O2浓度的两倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com