
| A. | 0.1 mol•L-1的CH3COOH | B. | 0.1 mol•L-1的NaHSO4 | ||
| C. | 0.1 mol•L-1的NaHCO3 | D. | 0.05 mol•L-1的H2SO3 |
分析 A、CH3COOH是一元弱酸,部分电离;
B、NaHSO4是强酸的酸式盐,酸式根离子完全电离;
C、NaHCO3是弱酸的酸式盐,酸式根离子部分电离;
D、H2SO3是二元弱酸,部分电离.
解答 解:A、CH3COOH是一元弱酸,部分电离,溶液中H+浓度为小于0.1mol•L-1,故A错误;
B、NaHSO4是强酸的酸式盐,酸式根离子完全电离,溶液中H+浓度为等于0.1mol•L-1,故B正确;
C、NaHCO3是弱酸的酸式盐,酸式根离子部分电离,溶液中H+浓度为小于0.1mol•L-1,故C错误;
D、H2SO3是二元弱酸,部分电离,溶液中H+浓度为小于0.1mol•L-1,故D错误;
故选B.
点评 本题通过考查电解质的强弱和酸的元数,来综合判断溶液中氢离子的浓度大小,难度不大.


科目:高中化学 来源: 题型:解答题
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 碱性的废水 | 用CO2中和 | 化学法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 废酸 | 加生石灰中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的本质特征是丁达尔效应 | |
| B. | 将小烧杯中25mL蒸馏水加至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热,可以制取Fe(OH)3胶体 | |
| C. | 溶液中分散质可通过滤纸,胶体中分散质不能通过滤纸 | |
| D. | 往Fe(OH)3胶体中逐滴加入稀H2SO4溶液时,开始时会出现凝聚,再继续逐滴加到过量时,沉淀也不会消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
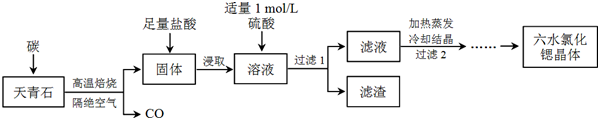
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离产生的c(H+)=10-12 mol/L的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 在c(H+)=$\sqrt{{K}_{W}}$mol/L的溶液中:K+、Fe3+、HCO3-、AlO2- | |
| C. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、SO42-、Cl- | |
| D. | pH=13的溶液中:NH4+、Na+、CO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水与稀盐酸反应:H++OH-═H2O | |
| B. | FeCl3溶液与铁反应:Fe3++Fe═2Fe2+ | |
| C. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| D. | KOH稀溶液中通入过量的SO2:SO2+OH-═HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减小、增大、减小 | B. | 增大、减小、减小 | C. | 减小、增大、增大 | D. | 增大、减小、增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com