
| A. | NaHCO3溶液:HCO3-+H2O?CO32-+H3O+ | |
| B. | NaHS溶液:HS-+H2O?H2S+OH- | |
| C. | Na2CO3溶液:CO32-+2H2O?H2CO3+2OH- | |
| D. | NH4Cl溶于D2O中:NH4++D2O?NH3•D2O+H+ |
分析 A.碳酸氢根水解生成碳酸和氢氧根离子;
B.硫氢根离子水解生成硫化氢和氢氧根离子;
C.碳酸根离子分步水解,以第一步为主;
D.铵根离子水解生成一水合氨和氢离子.
解答 解:A.NaHCO3溶液,离子方程式:HCO3-+H2O?H2CO3+OH-,故A错误;
B.NaHS溶液,离子方程式:HS-+H2O?H2S+OH-,故B正确;
C.Na2CO3溶液,离子方程式:CO32-+H2O?HCO3-+OH-,故C错误;
D.NH4Cl溶于D2O中,离子方程式:NH4++D2O?NH3•HDO+D+,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,侧重考查盐类水解的离子方程式,明确盐类水解规律是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 实验步骤 | 有关问题 |
| (1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为2.12g. |
| (2)称量Na2CO3固体 | 称量过程中应用到的主要仪器是分析天平或电子天平. |
| (3)将Na2CO3加入100mL烧杯中,加入适量蒸馏水 | 为了加快溶解速率,常采取的措施是用玻璃棒搅拌. |
| (4)将烧杯中的溶液转移至仪器A(已检查不漏水)中 | ①在转移Na2CO3溶液前应将溶液冷却至室温; ②仪器A是100mL容量瓶; ③为防止溶液溅出,应采取的措施是用玻璃棒引流. |
| (5)向仪器A中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是加蒸馏水至容量瓶中的液面接近刻度线1-2cm处,改用胶头滴管滴加至溶液的凹液面正好与刻度线相切. |
| (6)摇匀、装瓶,操作B,最后清洁、整理 | 操作B是贴标签. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 只有③ | B. | ②③ | C. | ①③⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(1)图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
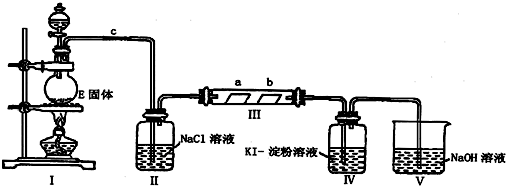
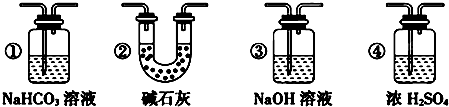
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个反应能否自发进行,由焓变、熵变、反应温度共同决定 | |
| B. | 在同一条件下,不同物质有不同的熵变,其体系混乱度越大,熵值越小 | |
| C. | 自发进行的反应一定能迅速发生 | |
| D. | 低温时,吸热且熵减的反应可能会自发发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com