
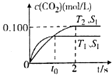
 ����β����������Ҫԭ��Ϊ2NO��g��+2CO��g��$\stackrel{����}{��}$2CO2+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ��ʾ���ݴ��жϣ�
����β����������Ҫԭ��Ϊ2NO��g��+2CO��g��$\stackrel{����}{��}$2CO2+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ��ʾ���ݴ��жϣ�| ������� | ��ʼ���ʵ��� | ƽ��ʱ���ʵ��� |
| �� | 2.0mol NO��2.0mol CO | 1.0mol CO2 |
| �� | 4.0mol NO��4.0mol CO |
���� ��1�����ݵ���ƽ���ʱ���ж��¶ȸߵͣ�����ƽ��ʱ������̼��Ũ���ж��¶ȶ�ƽ���Ӱ�죬�����жϷ�Ӧ����ЧӦ����ͼ��֪��T2�¶�ƽ��ʱ��������̼��Ũ�ȱ仯��Ϊ0.1mol/L������v=$\frac{��c}{��t}$����v��CO2�����ٸ�������֮�ȵ��ڻ�ѧ������֮�ȼ���v��N2����
��2���Ӵ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ��
��3���ٸ���K=$\frac{c��C{O}_{2}��^{2}c��{N}_{2}��}{{c}^{2}��NO��{c}^{2}��CO��}$���㣻�����ʱŨ����Qc=$\frac{c��C{O}_{2}��^{2}c��{N}_{2}��}{{c}^{2}��NO��{c}^{2}��CO��}$����Qc=K������ƽ��״̬����Qc��K����Ӧ������Ӧ���У���Qc��K����Ӧ���淴Ӧ���У�
�ڸ��ݵ�Чƽ���֪�����൱���ڢ�Ļ����ϼ�ѹ��ѹǿ����ƽ���������С�ķ����ƶ���������Ӧ�����ƶ���Ϊ���COת���ʣ���ƽ��������У���������NO���������¶ȣ�ѹǿ����
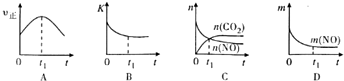
��4��A������ƽ���������������ȣ����ٱ仯��
B������ƽ����¶�Ϊ��ֵ��ƽ�ⳣ�����䣬��Ϸ�Ӧ���ж��淴Ӧ�����������¶ȱ仯���ж��¶ȶԻ�ѧƽ�ⳣ����Ӱ�죻
C������ƽ������ʵ����ʵ����������仯��
D������ƽ�����ֵĺ����������仯���������䣻
��5������G=��H-T•��S�жϷ�Ӧ�ܷ��Է����У�
��� �⣺��1����ͼ1��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�Խ��ƽ��ʱ��������̼��Ũ��Խ�ͣ�˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ����ͼ��֪��T2�¶�ʱ2s����ƽ�⣬ƽ��ʱ������̼��Ũ�ȱ仯��Ϊ0.2mol/L����v��CO2��=$\frac{0.2mol/L}{2s}$=0.1mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��N2��=$\frac{1}{2}$v��CO2��=$\frac{1}{2}$��0.1mol/��L•s��=0.05mol/��L•s����
�ʴ�Ϊ�����ȣ�0.05mol/��L•s����
��2���Ӵ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ����c��CO2����T1��S2�����´ﵽƽ������еı仯����Ϊ ��
��
�ʴ�Ϊ�� ��
��
��3���ٷ�Ӧ�ﵽƽ��״̬��������NO 1.0 mol/L��CO 1.0 mol/L��CO2 1.0 mol/L��N2 0.5mol/L��K=$\frac{c��C{O}_{2}��^{2}c��{N}_{2}��}{{c}^{2}��NO��{c}^{2}��CO��}$=$\frac{1.0{\;}^{2}•0.5}{1��{0}^{2}•1��{0}^{2}}$=0.5��
��ʼʱ���������г���1.0mol NO��1.5mol CO��2.0molCO2��0.5molN2��Ũ�ȷֱ�Ϊ��1.0 mol/L��1.5 mol/L��2.0 mol/L��0.5mol/L��Ũ����Qc=$\frac{c��C{O}_{2}��^{2}c��{N}_{2}��}{{c}^{2}��NO��{c}^{2}��CO��}$=$\frac{2��{0}^{2}•0.5}{1��{0}^{2}•1��{5}^{2}}$=0.89��0.5����Ӧ���淴Ӧ���У�
�ʴ�Ϊ��0.5���棻
�ڸ��ݵ�Чƽ���֪�����൱���ڢ�Ļ����ϼ�ѹ��ѹǿ����ƽ���������С�ķ����ƶ���������Ӧ�����ƶ���ת��������
Ϊ���COת���ʿɲ�ȡ�Ĵ�ʩ����������NO����ƽ��������У���Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ��������У�ѹǿ����ƽ��������У�
�ʴ�Ϊ������NO����ϵ��¶Ȼ�����ѹǿ��
�ʴ�Ϊ����������NO����ϵ��¶Ȼ�����ѹǿ��
��4��A������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮�����ʲ��䣬��A����
B���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬Ϊ��С��ͼ����ʵ�ʷ��ϣ���B��ȷ��
C��t1ʱ�̺�CO2��g����NO��g�������ʵ��������仯��t1ʱ��δ����ƽ��״̬����C����
D��t1ʱ�̣�NO��g��������Ϊ��ֵ������ƽ��״̬��ͼ����ʵ�ʷ��ϣ���D��ȷ��
��ѡ��BD��
��5��2CO��g��=2C��s��+O2��g�����÷�Ӧ���������ؼ��ķ�Ӧ������G=��H-T•��S��G��0������ʵ�֣�
�ʴ�Ϊ����H��0����S��0�������κ��¶��¡�G��0���������Է����У�
���� ���⿼���˻�ѧƽ�⡢ƽ�ⳣ������Ӧ����Ӱ�����ط����жϣ���ѧƽ����㣬��ѧƽ��Ľ������̷���Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=4��������pH=10�İ�ˮ��Һ�������Ϻ�pH��7 | |
| B�� | ��ˮ�У�c��Cl2��=2[c��ClO-��+c��Cl-��+c��HClO��] | |
| C�� | pH=11��NaOH��pH=11�İ�ˮ�ֱ�ϡ��100�����pHǰ��һ�����ں��� | |
| D�� | 0.10 mol•L-1 Na2CO3��Һ��c��Na+��+c��H+��=c��OH-��+c��HCO3-��+c��CO32-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | ��NH4��2SO4 | C�� | Na2O | D�� | CH3COONa |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
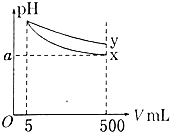 pH=11��x��y���ּ���Һ��5ml���ֱ�ϡ����500ml����pH����Һ�����V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
pH=11��x��y���ּ���Һ��5ml���ֱ�ϡ����500ml����pH����Һ�����V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | x��ǿ�y������ | |
| B�� | ��x��y��һԪ�������ʵ���Ũ�ȵ�x����������Һ��pH��y����������Һ�� | |
| C�� | ��x��y��һԪ�������pH=11��x��y���ּ���Һ��Ũ����ͬ | |
| D�� | ��ȫ�к�x��y����Һʱ������ͬŨ��ϡ��������V��x����V��y�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | þ�����ᷴӦ�ų����� | B�� | ������طֽ� | ||
| C�� | ��������������ķ�Ӧ | D�� | Ba��OH��2•8H2O��NH4Cl��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
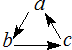 ���и��������У�����֮��ͨ��һ����Ӧ����ʵ����ͼ��ʾת�����ǣ�������
���и��������У�����֮��ͨ��һ����Ӧ����ʵ����ͼ��ʾת�����ǣ�������| a | b | c | |
| A | Cl2 | HClO | HCl |
| B | Si | SiO2 | H2SiO3 |
| C | Cu | CuSO4 | Cu��OH��2 |
| D | Na | NaOH | NaHCO3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
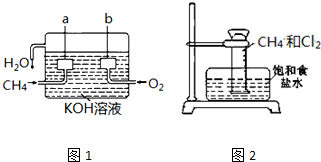
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com