
| A. | Cu2+、Mg2+、SO42-、NO3- | B. | H+、Mg2+、SO42-、HCO3- | ||
| C. | Ag+、Na+、NO3-、Cl- | D. | NH4+、Ba2+、NO3-、OH- |
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:解答题
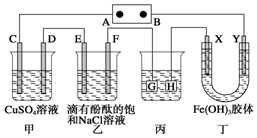 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入过量SO2:H+、Cl-、ClO-、HSO3- | |
| B. | 通入过量FeSO4溶液:Fe2+、H+SO42-、ClO- | |
| C. | 加入少量Al2(SO4)3溶液:Al3+、H+、ClO-、SO42- | |
| D. | 加入少量Na2O2固体:Na+、Cl-、ClO-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中存在:[Na+]+[H+]=2[CO32-]+[HCO3-]+[OH-] | |
| B. | 若二者等物质的量混合,则溶液中[CO32-]=[HCO3-] | |
| C. | 该溶液中[H+]=Ka2[HCO3-]/[CO32-](Ka2为H2CO3的二级电离常数) | |
| D. | 该溶液加少量水稀释pH不发生明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.02mol/L的NaOH溶液与0.04mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)=c(HC2O4)+2c(H+) | |
| C. | 叠氨酸(NH3)与醋酸酸性相近,0.1mol•L-1 NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| D. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “曾青涂铁”属于湿法炼铜 | |
| B. | “曾青涂铁”发生的是铁与硫酸铜的反应 | |
| C. | 汞不能用湿法冶炼 | |
| D. | “丹砂烧之成水银”属于热分解法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验序号 | 甲 | 乙 | 丙 |
| 混合物质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 类别 选项 | 纯净物 | 混合物 | 电解质 |
| A | 生理盐水 | 明矾 | 液态KNO3 |
| B | CaO | 海 水 | 铜 |
| C | 胆矾 | 铝合金 | AgNO3 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | ① | ② | ③ |
| 溶液 | NaClO | NaHCO3 | Na2CO3 |
| pH | 10.3 | 8.3 | 11.6 |
| A. | 酸性:HClO>H2CO3 | |
| B. | 由水电离产生的c(OH-):①>② | |
| C. | 溶液①中的c(ClO-)大于溶液②中的c(HCO3-) | |
| D. | 溶液③中:c(HCO3-)+c(CO32-)=0.1 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com