
 Si3N4+ CO
Si3N4+ CO科目:高中化学 来源:不详 题型:填空题
 ol)随时间t的变化如右图所示,已知达平衡后,降低温度,A的转化率将增大。
ol)随时间t的变化如右图所示,已知达平衡后,降低温度,A的转化率将增大。

 |  |  |  |
 |  |  |  |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C +2D达到平衡
2C +2D达到平衡查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.在石英管右端主要物质是Ni(CO)4(g) |
| B.在石英管右端主要物质是纯Ni(s)和CO(g) |
| C.在石英管左端主要物质是纯Ni(s)和CO(g) |
| D.整个过程可以看作CO(g)将Ni(s)从石英管左端转移到右端,从而达到提纯目的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
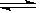 2C(g)达
2C(g)达 到平衡的是()
到平衡的是() ①C的生成速率与C的分解速率相等;②单位时间生成amol A,同时生
①C的生成速率与C的分解速率相等;②单位时间生成amol A,同时生 成3amolB;③A、B、C的浓度不再变化;④A、B、C的物质的量不再变化;
成3amolB;③A、B、C的浓度不再变化;④A、B、C的物质的量不再变化; ⑤混合气体的总压强不再变化;⑥混合气体的总物质的量不再变化;⑦单位时间消耗amol A,同时生成3amol B;⑧A、B、C的分子数目比为1:3:2。
⑤混合气体的总压强不再变化;⑥混合气体的总物质的量不再变化;⑦单位时间消耗amol A,同时生成3amol B;⑧A、B、C的分子数目比为1:3:2。 A.②⑧ B.⑦④ C.①③ D.⑤⑥
A.②⑧ B.⑦④ C.①③ D.⑤⑥查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3,下列说法中,能充分说明这一反应已经达到化学平衡状态的是( )
2NH3,下列说法中,能充分说明这一反应已经达到化学平衡状态的是( )| A.N2、H2与NH3的物质的量之比为1︰3︰2 | B.N2、H2与NH3的浓度相等 |
| C.各组分的浓度不再发生变化 | D.反应停止,正、逆反应速率都等于零 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中正确的是
c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中正确的是| A.平衡向逆反应方向移动 | B.a+b>c+d |
| C.W的体积分数增大 | D.X的转化率降低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.达到化学反应平衡时,生成的NH3为2mol |
| B.达到化学反应平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C.达到化学反应平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D.达到化学反应平衡时,正反应和逆反应的速率都为零 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2X(g)+Y(g)
2X(g)+Y(g) 3R(g),该反应经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是( )
3R(g),该反应经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是( )| A.用物质X表示该反应在2s内的平均反应速率为0.2 mol/(L·s) |
| B.其他条件不变,向容器中再加入l mol R气体,达到新的平衡后,R的体积分数不变 |
C.其他条件不变,加压缩小容器体积时平衡不移动,气体密度和平均相对分子质量均增大 |
D.平衡时物质X与Y的转化率相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com