
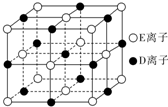
 A”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ×īĒ棻F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£®GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£®
A”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ×īĒ棻F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£®GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£®·ÖĪö A”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£¬ŌņĘäŌ×ÓŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p2£¬¹ŹAĪŖCŌŖĖŲ£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£¬ŌņDĪŖNaŌŖĖŲ£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£¬“¦ÓŚ¢öA×壬½įŗĻŌ×ÓŠņŹżæÉÖŖCĪŖOŌŖĖŲ£¬¹ŹBĪŖNŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌ×īĒ棬ŌņEĪŖCl£¬F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£¬F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£¬Ō×ÓŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p63s23p63d104s1£¬ŌņFĪŖCu£»GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£¬ŌņGĪŖCs£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£¬ŌņĘäŌ×ÓŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p2£¬¹ŹAĪŖCŌŖĖŲ£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£¬ŌņDĪŖNaŌŖĖŲ£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£¬“¦ÓŚ¢öA×壬½įŗĻŌ×ÓŠņŹżæÉÖŖCĪŖOŌŖĖŲ£¬¹ŹBĪŖNŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌ×īĒ棬ŌņEĪŖCl£¬F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£¬F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£¬Ō×ÓŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p63s23p63d104s1£¬ŌņFĪŖCu£»GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£¬ŌņGĪŖCs£¬
£Ø1£©øßĀČĖįµÄĖįŠŌ±ČĻõĖįĒ棬ŌŅņŹĒøßĀČĖį·Ö×ÓÖŠ·ĒōĒ»łŃõŹżÄæ¶ąÓŚĻõĖį·Ö×Ó£¬µ¼ÖĀøßĀČĖįÖŠCl-O-HÖŠµē×Ó¶Ōøü¼ÓĘ«ĻņÓŚCl£¬Ņņ¶ųŌŚĖ®·Ö×ÓµÄ×÷ÓĆĻĀ£¬øßĀČĖįøüČŻŅ×µēĄė³öH+£¬¹ŹøßĀČĖįĖįŠŌĒ棬
¹Ź“š°øĪŖ£ŗøßĀČĖį·Ö×ÓÖŠ·ĒōĒ»łŃõŹżÄæ¶ąÓŚĻõĖį·Ö×Ó£¬µ¼ÖĀøßĀČĖįÖŠCl-O-HÖŠµē×Ó¶Ōøü¼ÓĘ«ĻņÓŚCl£¬Ņņ¶ųŌŚĖ®·Ö×ÓµÄ×÷ÓĆĻĀ£¬øßĀČĖįøüČŻŅ×µēĄė³öH+£¬¹ŹøßĀČĖįĖįŠŌĒ棻
£Ø2£©FĪŖCu£¬¶ŌÓ¦µÄ¾§ĢåĪŖĆęŠÄĮ¢·½×īĆܶѻż£¬¹Ź“š°øĪŖ£ŗĆęŠÄĮ¢·½×īĆܶѻż£»
£Ø3£©NaCl”¢CsClĮ½ÖÖ¾§Ģ壬¶¼ŹōÓŚĄė×Ó¾§Ģ壬ÓÉÓŚÕżøŗĄė×ӵİė¾¶±Č²»Ķ¬£¬¹ŹĖüĆĒµÄÅäĪ»Źż²»Ķ¬£¬¹Ź“š°øĪŖ£ŗŅõŃōĄė×Ó°ė¾¶±Č²»Ķ¬£»
£Ø4£©NaCl¾§ĢåµÄ¾§°ūÖŠµÄĖłÓŠCl-Ąė×ÓČ„µō£¬²¢½«Cl-Ąė×ÓČ«²æ»»ĪŖC£ØĢ¼£©Ō×Ó£¬ŌŁŌŚĘäÖŠµÄ4øö”°Š” Į¢·½Ģå”±ÖŠŠÄø÷·ÅÖĆŅ»øöC£ØĢ¼£©Ō×Ó£¬ĒŅÕā4øö”°Š”Į¢·½Ģå”±²»ĻąĮŚ£®Ī»ÓŚ”°Š”Į¢·½Ģå”±ÖŠµÄCŌ×ÓÓė×ī½üµÄ4øöCŌ×ÓŅŌµ„¼üĻąĮ¬£¬ŠĪ³ÉÕżĖÄĆęĢå½į¹¹£¬¾§°ūÖŠC£ØĢ¼£©Ō×ÓŹżÄæ=4+8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=8£¬¾§°ūÖŹĮæ=8”Į$\frac{12g}{{N}_{A}}$£¬C-C¼üµÄ¼ü³¤ ĪŖa cm£¬ČēĶ¼ÕżĖÄĆęĢå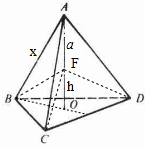 £¬Į¬½ÓFÓėA”¢B”¢C”¢D£¬ŌņČżĄā׶A-BCD¾ł·ÖĪŖµČ4øöµČĢå»żµÄČżĄā×µ£¬ŌņVČżĄā׶A-BCD=4VČżĄā׶F-BCD=£¬¹Ź$\frac{1}{3}$S”÷BCD•£Øa+h£©=4”Į$\frac{1}{3}$S”÷BCD•h£¬¹Źh=$\frac{1}{3}$a£¬ĮīÕżĖÄĆęĢåµÄĄā³¤ĪŖx cm£¬Į¬½ÓAF²¢ŃÓ³¤½»Čż½ĒŠĪBCDÓėO£¬OĪŖÕżČż½ĒŠĪBCDµÄÖŠŠÄ£¬BO“¹Ö±Ę½·ÖCD£¬ŌņBOµÄ³¤¶Č=x cm”Į$\frac{\sqrt{3}}{2}”Į\frac{2}{3}$=$\frac{\sqrt{3}}{3}$xcm£¬ŌŚÖ±½ĒČż½ĒŠĪBOFÖŠ£¬$£Ø\frac{\sqrt{3}}{3}x£©^{2}+£Ø\frac{1}{3}a£©^{2}$=a2£¬½āµĆx=$\frac{2\sqrt{6}a}{3}$¹Ź¾§°ūµÄĄā³¤=$\frac{\sqrt{2}}{2}$”Į2xcm=$\frac{\sqrt{2}}{2}”Į2”Į\frac{2\sqrt{6}a}{3}$cm=$\frac{4\sqrt{3}a}{3}$cm£¬¹Ź¾§°ūµÄĢå»ż=$£Ø\frac{4\sqrt{3}}{3}a£©^{3}$=$\frac{64}{3\sqrt{3}}{a}^{3}$cm3£¬Ōņ¾§°ūĆܶČ=$\frac{8”Į\frac{12g}{{N}_{A}}}{\frac{64}{3\sqrt{3}}{a}^{3}}$=$\frac{9\sqrt{3}}{2{a}^{3}{N}_{A}}$g•cm-3£¬
£¬Į¬½ÓFÓėA”¢B”¢C”¢D£¬ŌņČżĄā׶A-BCD¾ł·ÖĪŖµČ4øöµČĢå»żµÄČżĄā×µ£¬ŌņVČżĄā׶A-BCD=4VČżĄā׶F-BCD=£¬¹Ź$\frac{1}{3}$S”÷BCD•£Øa+h£©=4”Į$\frac{1}{3}$S”÷BCD•h£¬¹Źh=$\frac{1}{3}$a£¬ĮīÕżĖÄĆęĢåµÄĄā³¤ĪŖx cm£¬Į¬½ÓAF²¢ŃÓ³¤½»Čż½ĒŠĪBCDÓėO£¬OĪŖÕżČż½ĒŠĪBCDµÄÖŠŠÄ£¬BO“¹Ö±Ę½·ÖCD£¬ŌņBOµÄ³¤¶Č=x cm”Į$\frac{\sqrt{3}}{2}”Į\frac{2}{3}$=$\frac{\sqrt{3}}{3}$xcm£¬ŌŚÖ±½ĒČż½ĒŠĪBOFÖŠ£¬$£Ø\frac{\sqrt{3}}{3}x£©^{2}+£Ø\frac{1}{3}a£©^{2}$=a2£¬½āµĆx=$\frac{2\sqrt{6}a}{3}$¹Ź¾§°ūµÄĄā³¤=$\frac{\sqrt{2}}{2}$”Į2xcm=$\frac{\sqrt{2}}{2}”Į2”Į\frac{2\sqrt{6}a}{3}$cm=$\frac{4\sqrt{3}a}{3}$cm£¬¹Ź¾§°ūµÄĢå»ż=$£Ø\frac{4\sqrt{3}}{3}a£©^{3}$=$\frac{64}{3\sqrt{3}}{a}^{3}$cm3£¬Ōņ¾§°ūĆܶČ=$\frac{8”Į\frac{12g}{{N}_{A}}}{\frac{64}{3\sqrt{3}}{a}^{3}}$=$\frac{9\sqrt{3}}{2{a}^{3}{N}_{A}}$g•cm-3£¬
¹Ź“š°øĪŖ£ŗ8£»$\frac{9\sqrt{3}}{2{a}^{3}{N}_{A}}$£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ½į¹¹ÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪö”¢¼ĘĖćÄÜĮ¦µÄ漲飬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬×¢ŅāÕĘĪÕŌŖĖŲÖÜĘŚĀÉ£¬£Ø4£©ÖŠĆÜ¶Č¼ĘĖćĪŖŅדķµć”¢ÄŃµć£¬ŠčŅŖѧɜ¾ß±øŅ»¶ØµÄŹéŠ“¼ĘĖćÄÜĮ¦£¬ÄŃ¶Č½Ļ“ó£®


 ĘÕĶØøßÖŠĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ĘÕĶØøßÖŠĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
ÓÅŅķŠ”°ļŹÖĶ¬²½æŚĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
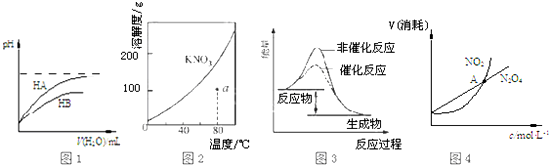
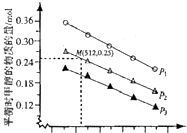
| A£® | Ķ¼1±ķŹ¾³£ĪĀĻĀ£¬Ļ”ŹĶHA”¢HBĮ½ÖÖĖįµÄĻ”ČÜŅŗŹ±£¬ČÜŅŗpHĖę¼ÓĖ®ĮæµÄ±ä»Æ£¬ŌņNaAČÜŅŗµÄpHŠ”ÓŚĶ¬ÅØ¶ČµÄNaBČÜŅŗµÄpH | |
| B£® | Ķ¼2±ķŹ¾ KNO3µÄČܽā¶ČĒśĻߣ¬aµćĖłŹ¾µÄČÜŅŗŹĒ80”ꏱKNO3µÄ²»±„ŗĶČÜŅŗ | |
| C£® | Ķ¼3 ±ķŹ¾Ä³·ÅČČ·“Ó¦·Ö±šŌŚÓŠ”¢ĪŽ“߻ƼĮµÄĒéæöĻĀ·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ | |
| D£® | Ķ¼4±ķŹ¾ŗćĪĀŗćČŻĢõ¼žĻĀ£¬2NO2£Øg£©?N2O4£Øg£©ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ü¢Ż | C£® | ¢Ū¢Ü¢Ż | D£® | ¢Ł¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ±ķŹ¾µÄ·Ö×ÓŹ½ĪŖC6H14£»Ćū³ĘŹĒ2-¼×»łĪģĶ飮
±ķŹ¾µÄ·Ö×ÓŹ½ĪŖC6H14£»Ćū³ĘŹĒ2-¼×»łĪģĶ飮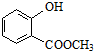 ÖŠŗ¬ÓŠµÄ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł”¢õ„»ł£®
ÖŠŗ¬ÓŠµÄ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł”¢õ„»ł£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
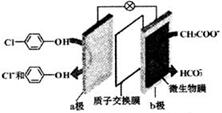 ĄūÓĆĪ¢ÉśĪļµē³Ų“¦Ąķŗ¬ŅŅĖįÄĘŗĶ¶ŌĀČ·Ó£Ø
ĄūÓĆĪ¢ÉśĪļµē³Ų“¦Ąķŗ¬ŅŅĖįÄĘŗĶ¶ŌĀČ·Ó£Ø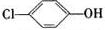 £©µÄ·ĻĖ®£¬¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
£©µÄ·ĻĖ®£¬¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | µē¼«bŹĒÕż¼« | B£® | ÖŹ×Ó“Óa¼«ŅĘĻņb¼« | ||
| C£® | “¦ĄķŗóµÄ·ĻĖ®pHÉżøß | D£® | a¼«µÄµē¼«·“Ó¦Ź½£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »Æѧ¼ü | C=0 | H-H | C-C | C-H | 0-H | C-0 |
| ¼üÄÜ/kJ•mol-1 | 803 | 436 | 332 | 409 | 463 | 326 |
| ³É·Ö | ŗ¬Įæ/£Ømg/L£© | ³É·Ö | ŗ¬Įæ£Ømg/L£© |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3-£» | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
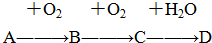
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com