
【题目】某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO![]() +H2O。下列说法正确的是
+H2O。下列说法正确的是
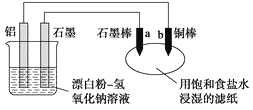
A. 电池的负极反应式为:ClO-+H2O+2e-=Cl-+2OH-
B. 当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个
C. 往滤纸上滴加酚酞试液,b极附近颜色变红
D. b极附近会生成蓝色固体
【答案】C
【解析】
A.电池的正极反应式为:ClO-+H2O+2e-=Cl-+2OH-,错误;
B.电池的负极反应式为:Al-3e-+4OH-=AlO2-+2H2O,当有0.1 mol Al完全溶解时,流经外电路的电子数为1.806×1023个,而在电解质溶液中则是离子定向移动,错误;
C.往滤纸上滴加酚酞试液,由于Al是负极,所以b极为阴极,在该电极上溶液中的H+放电,破坏了b极附近的水的电离平衡,使该区域的溶液显碱性,所以b电极附近颜色变红,正确;
D.由于Al是负极,所以与之连接的b极是阴极,b极的电极反应式为2H2O+2e-=H2↑+2OH-,Cu棒不参与反应,所以b极附近不会生成蓝色固体,错误;
答案选C。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,1个氧气分子体积为 ![]() cm3
cm3
B.铜电解精炼时,当阳极质量减少64 g时,电路中转移电子数为2NA
C.标准状况下22.4 L Cl2完全溶于水时,所得溶液中含氯微粒总数为2NA
D.NaCl晶体中Na+与最近Cl-的核间距离为a cm,则其晶体密度为 ![]() g·cm-3
g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不能够用勒夏特勒原理来解释的是
A. 实验室用排饱和食盐水的方法收集氯气
B. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后(AgBr是淡黄色沉淀),溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后(AgBr是淡黄色沉淀),溶液颜色变浅
C. SO2催化氧化制SO3的过程中使用过量的氧气,以提高二氧化硫的转化率
D. 恒温、恒压条件下,在2NO2![]() N2O4平衡体系中充入He后,体系颜色变浅
N2O4平衡体系中充入He后,体系颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时 H2A 的pKa1=1.85,pKa2=7.19。常温下,用 0.1mol·L-1NaOH 溶封液滴定 20 mL 0.1 mol·L-1H2A 溶液的滴定曲线如图所示。下列说法不正确的是

A.A 点 V0﹤10 mL线
B.B 点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
C.C 点所得溶液中:c(A2-)=c(HA-)
D.D 点所得溶液中:A2-水解平衡常数Kh1=10-6.81
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到___________(填仪器名称)中定容,摇匀即得。
(2)用________取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴___作指示剂。
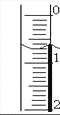
(3)读取盛装0.1000 mol/L NaOH 溶液的___________(填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为_________mL。
(4)滴定。当______________________________________________时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)经计算,市售白醋总酸量=_____________g/100mL。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是______(填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物 L(![]() )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:
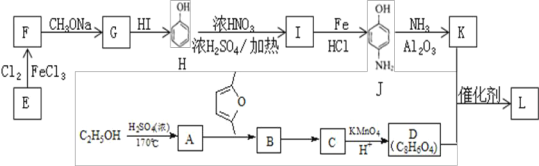
已知:①C、D、K 均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels﹣Alder 反应![]() +
+![]()
![]()
![]()
③ R2Cl![]() R1OR2
R1OR2
(1)I→J 的反应类型是________,D 的名称是________,G 中所含官能团的名称是________。
(2)B 的结构简式是________,“B→C”的反应中,除 C 外,另外一种产物是________。
(3)D+K→L 的化学方程式是________。
(4)M 为 D 的同分异构体,同时满足下列条件的 M 的结构简式为________。
①1 molM 最多消耗 4 mol NaOH ②核磁共振氢谱有 4 组吸收峰
(5)N 是 D 的同系物,相对分子质量比 D 大 14,则 N 可能的结构有________种。
(6)已知:乙炔与 1,3﹣丁二烯也能发生 Diels﹣Alder 反应。请以 1,3﹣丁二烯和乙炔为原料,选用必要的无机试剂合成 ,写出合成路线:________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线:________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
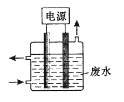
A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C. 阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D. 除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + 5Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是制备精盐的实验方案,各步操作流程如下:

(1)第②步操作的目的是除去粗盐中的______(填化学式)。
(2)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、___(填化学式)。
(3)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是________。
(4)写出第⑥步反应的离子方程式_______________,______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物中,可能含有下列离子中的几种:K+、NH4+、Mg2+、Ba2+、Cl-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取三份各100mL该溶液分别进行如下实验:
(1)在一份溶液中加入AgNO3溶液,有白色沉淀生成;
(2)在另一份溶液中加入足量的NaOH溶液并加热,收集到1.12L气体(标准状况下);
(3)在第三份溶液中加入足量的BaCl2溶液有沉淀生成,经称量其质量为6.27g,在该沉淀中 加入足量的盐酸,沉淀部分溶解,剩余固体质量为2.33g。
根据上述实验回答下列问题:
①溶液中一定不存在的离子是:_______________________________;
②溶液中一定存在的阴离子有:_______________;其物质的量浓度分别为:_____________;
③推断K+是否存在:(填“是 ”或“否”)________________,其物质的量浓度为:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com