
【题目】电化学原理在化学工业中有广泛的应用。请根据如图回答问题:
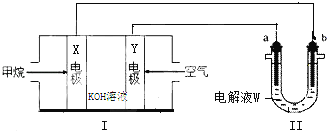
(1)装置Ⅰ中的X电极的名称是____________,Y电极的电极反应式为________,工作一段时间后,电解液的pH将________(填“增大”、“减小”、“不变”)。
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示)___________,a电极上有气泡产生,该气体的电子式为____。
(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为_______________,工作一段时间后装置Ⅱ电解液中c(Cu2+)将_______________(填“增大”、“减小”、“不变”)。
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.1.6g,则流经电路的电子的物质的量为___________________。
【答案】负极 O2+2H2O+4e﹣=4OH﹣ 减小 2H++2e﹣=H2↑或2H2O+2e﹣=H2↑+2OH﹣ ![]() 粗铜 减小 0.02mol
粗铜 减小 0.02mol
【解析】
(1)装置Ⅰ为甲烷燃料电池,燃料在负极发生氧化反应,生成二氧化碳能够与KOH反应,导致溶液pH减小,在碱性环境中,氧气在正极发生还原反应,生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-;
(2)电解饱和食盐水得到氢气、氯气和氢氧化钠,其离子方程式为:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-,b是阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧化钠,所以溶液碱性增强,酚酞试液遇碱变红色,电极反应式为:2H++2e-=H2↑,氯气的电子式为
H2↑+Cl2↑+2OH-,b是阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧化钠,所以溶液碱性增强,酚酞试液遇碱变红色,电极反应式为:2H++2e-=H2↑,氯气的电子式为![]() ;
;
(3)电镀法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,为阳极a电极连接粗铜,电解一段时间后,溶液中铜离子浓度在减小;
(4)铜棒是阴极,银离子放电,生成n(Ag)=![]() =0.02mol,转移电子0.02mol。
=0.02mol,转移电子0.02mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】为了社会可持续发展,化工生产过程应尽量减少对环境的副作用。“绿色化学”是当今社会提出的一个新概念,它要求从经济、环保和技术上设计可行的化学反应,据此,由单质铜制取硝酸铜的下列衍变关系可行且符合“绿色化学”的是( )
A.Cu![]() Cu(NO3)2
Cu(NO3)2
B.Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
C.Cu![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2![]() Cu(NO3)2
Cu(NO3)2
D.Cu![]() CuSO4
CuSO4![]() 2Cu(NO3)2
2Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200℃时,将a mol H2(g)和b mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)2HI(g)。
(1)反应刚开始时,由于c(H2)=______,c(I2)=______,而c(HI)=________,所以化学反应速率________最大而________最小(为零)(填“v正”或“v逆”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)________,c(I2)________,而c(HI)________,从而化学反应速率v正________,而v逆________(填“增大”、“减小”或“不变”)。
(3)当反应进行到v正与v逆________时,此可逆反应就达到了最大限度,若保持外界条件不变时,混合物中各组分的物质的量、物质的量浓度、质量分数、体积分数、反应物的转化率和生成物的产率及体系的总压强(或各组分的分压)都将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中先加入氯水再加入KSCN溶液 | 溶液呈红色 | 原溶液中一定含 |
B | 向盛有 | 试管口出现红棕色气体 |
|
C | 向 | 出现白色胶状沉淀 | 碳的非金属性强于硅的 |
D | 用一束强光照射淀粉溶液 | 产生光亮的“通路” | 淀粉发生水解生成了胶体 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同
B.配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C.用加热的方法可以除去KCl溶液中的Fe3+
D.为抑制Fe3+的水解,较好地保存FeCl3溶液,应加少量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是( )
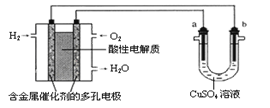
A. 燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH-
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入 6mol/L 的硫酸溶液,乙同学将电极放入 6mol/L 的氢氧化钠溶液中,如图所示:

(1)写出甲电池中正极的电极反应式___________________ ;
(2)写出乙池中负极的电极反应式: 负极:_____ 总反应的离子方程式:_________
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金 属,则构成负极材料的金属活泼
,则甲会判断出_____活动性更强,而乙会判断出_____活动性更强(填名称)
(4)由此实验,可得到如下哪些正确结论(_____)
a. 利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b. 镁的金属性不一定比铝的强
c. 该实验说明金属活动性顺序表已过时,已没有利用价值
d. 该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动性顺序表判断原电池中的正负极”这种做法__填 “可靠”或“不可靠”)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案_______________ (如 可靠,可不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油产品含有多种含硫物质,如H2S、COS等。
(1)一种脱硫工艺为:真空K2CO3-克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为1gK=___。
(已知:H2CO3 lgK1=-6.4, lgK2=-10.3;H2S 1gK1=-7,lgK2=-19)
②已知下列热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1 =-1172kJ·mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2 =-632kJ·mol-1
克劳斯法回收硫的反应为SO2气体和H2S气体反应生成S(s),则该反应的热化学方程式为___________________。同时,COS发生水解反应: COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H>0,结合以上两个反应,克劳斯法选择反应温度为300℃,温度低有利于____,但温度过低会使硫析出,降低催化剂活性,反应过慢,以及不利于_______________。
CO2(g)+H2S(g) △H>0,结合以上两个反应,克劳斯法选择反应温度为300℃,温度低有利于____,但温度过低会使硫析出,降低催化剂活性,反应过慢,以及不利于_______________。
(2)石灰石料浆作为脱硫剂可有效吸收废气中的SO2,将CO2气体通入石灰石料浆罐对CaCO3脱硫剂进行活化处理可明显提高CaCO3脱硫的效率,活化后的主要脱硫反应之一为:2Ca2++2SO2+O2+3H2O = 2CaSO4·![]() H2O+4H+。
H2O+4H+。
①废气经脱硫后,除水蒸气外,________(填气体化学式)含量明显增多。
②其他条件一定,物料比为1.2时,脱硫反应的速率受Ca2+浓度的影响。图中a点是Ca(OH)2为脱硫剂时的脱硫效率,曲线表示CaCO3活化时间对脱硫效率的影响。
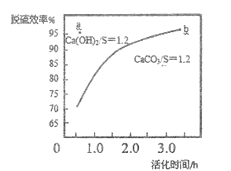
I.CaCO3与SO2反应的速率明显低于Ca(OH)2与SO2反应的速率,其原因是________。
II.a点和b点脱硫效率接近的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《战争的气体化学和分析》中介绍了一种制取rad(光气,熔点为-118℃,沸点为8.2℃,微溶于水,易溶于甲苯等有机溶剂)的方法,其实验装置如图所示(夹持装置已省略),下列说法正确的是( )
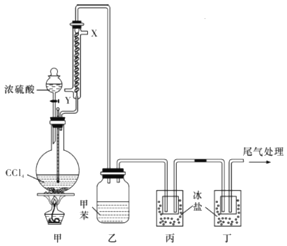
A.该反应属于氧化还原反应
B.自来水从冷凝管的X 口通入
C.可将装置丁的尾气通过导管直接通入NaOH溶液中进行尾气处理
D.装置乙中可收集到光气的甲苯溶液,装置丙、丁中均可收集到液态光气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com