
| A. | 品红溶液 | B. | 澄清石灰水 | C. | 紫色石蕊试液 | D. | 高锰酸钾溶液 |
分析 SO2与CO2都是酸性氧化物,SO2和CO2气体都可使澄清石灰水变浑浊,SO2具有还原性和漂白性,以此解答该题.
解答 解:A.二氧化硫具有漂白性,能够使品红褪色,可鉴别,故A正确;
B.SO2与CO2都是酸性氧化物,SO2和CO2气体都可使澄清石灰水变浑浊,不能鉴别,故B错误;
C.SO2与CO2都是酸性氧化物,与水反应生成碳酸和亚硫酸,SO2和CO2气体都可使紫色石蕊试液变红,不能鉴别,故C错误;
D.二氧化碳与高锰酸钾不反应,二氧化硫具有还原性,与高锰酸钾发生氧化还原反应使其褪色,现象不同,可鉴别,故D正确.
故选AD.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、性质差异及发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| B. | 标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子 | |
| C. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3 NA | |
| D. | 常温下,1L 0.1 mol•L-1的Na2CO3溶液中含有的离子总数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
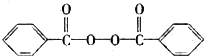
 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式: ;
;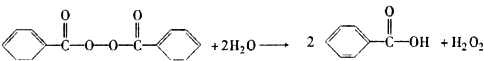
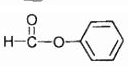 ,属于酚类结构的同分异构体有3种.
,属于酚类结构的同分异构体有3种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: | |
| B. | 氟化氢的形成过程: | |
| C. | 表示甲烷分子和四氯化碳分子的比例模型: | |
| D. | 次氯酸的结构式:H-O-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在潮湿的空气中放置不易生锈 | B. | 硬度比生铁大 | ||
| C. | 与2mol/L盐酸的反应生成氢气 | D. | 在冷的浓H2SO4溶液中可钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li在氧气中燃烧主要生成Li2O | |
| B. | 卤族元素单质X2(X:代表F、Cl、Br、I)均可以与水反应生成HX | |
| C. | 将SO2通入次氯酸钙溶液可能得到次氯酸 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64 g SO2含有氧原子数为NA | |
| B. | 1 mol铁与足量稀盐酸反应转移的电子数目为3 NA | |
| C. | 在同温同压下,相同体积的任何气体单质应含有相同的原子数 | |
| D. | 常温常压下,14 g N2含有分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+和Cu2+ | B. | Fe3+ | C. | Cu2+ | D. | Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com