
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)
该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,则10 min内CO2的平均反应速率为0.015 mol/(L·min),10 min后生成了单质铁________g。
(2)可用上述反应中某种物理量来说明该反应已达到平衡状态的是______________。
A.CO的生成速率与CO2的生成速率相等
B.CO生成速率与CO2消耗速率相等
C.CO的质量不变
D.体系的压强不再发生变化
E.气体密度不再变化
(3)写出氢氧化铝在水中发生酸式电离的电离方程式;
________________________________________________________________________。
欲使上述体系中H+浓度增大,可加入的物质是________。
A.NaOH B.HCl
C.NH3 D.NaHSO4
解析:(1)10 min内生成CO2的物质的量为0.015 mol/(L·min)×10 min×2 L=0.3 mol,由以下关系式
2Fe ~ 3CO2
2 mol 3 mol
0.2 mol 0.3 mol
m(Fe)=0.2 mol×56 g/mol=11.2 g。
(2)CO生成速率为逆反应速率,CO2生成速率为正反应速率,且CO、CO2前的化学计量数相等,则v(CO2)正=v(CO)逆,达到化学平衡;v(CO)生成=v(CO)逆,v(CO2)消耗=v(CO2)逆,无法说明是否达到化学平衡;m(CO)不变,则n(CO)不变,反应达到平衡; 该反应是气体体积不变的反应,反应任意时刻,体系的压强均相同;ρ=
该反应是气体体积不变的反应,反应任意时刻,体系的压强均相同;ρ= ,当m(气体)不变时,反应即达到平衡。
,当m(气体)不变时,反应即达到平衡。
(3)Al(OH)3 AlO
AlO +H++H2O,c(H+)增大,平衡正向移动,但A、C都能与H+反应,则B、D物质为可选项,虽然加入HCl、NaHSO4时,平衡逆向移动,但外加试剂中含有H+,使c(H+)增大。
+H++H2O,c(H+)增大,平衡正向移动,但A、C都能与H+反应,则B、D物质为可选项,虽然加入HCl、NaHSO4时,平衡逆向移动,但外加试剂中含有H+,使c(H+)增大。
答案:(1)11.2 (2)ACE
(3)Al(OH)3 H++AlO
H++AlO +H2O BD
+H2O BD


科目:高中化学 来源: 题型:
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.(b-a)/V mol·L-1
B.(2b-a)/V mol·L-1
C.2(b-a)/V mol·L-1
D.2(2b-a)/V mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )

| 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红色 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
| C | 石蕊溶液先变为红色后褪色 | Cl2具有漂白性 |
| D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器内,800℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度是__________;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
(2)如图中表示NO2变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
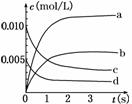
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是( )
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是( )

A.b代表0 ℃下CH3COCH3的Y-t曲线
B.反应进行到20 min末,CH3COCH3的 >1
>1
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 =1
=1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液中的电离方程式错误的是
A.NaHCO3===Na++H++CO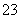
B.NaHSO4===Na++H++SO
C.MgCl2===Mg2++2Cl-
D.Ba(OH)2===Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如下图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是

A.OH-+HCl===H2O+Cl-
B.Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C.Fe+Cu2+===Cu+Fe2+
D.Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是: ( )
A.汽油燃烧时将全部的化学能转化为热能
B.向饱和AgCl溶液中加入盐酸,Ksp变大
C.若存在简单阴离子R2-,则R一定属于VIA族
D.最外层电子数少的金属元素,一定比最外层电子数多的金属元素活泼性强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com