


科目:高中化学 来源: 题型:


| aV1-0.5bV 2 |
| 1000 |
| aV1-0.5bV 2 |
| 1000 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
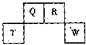 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
①2FeCl2+Cl2=2FeCl3 ②2FeCl3+2KI=2FeCl2+2KCl+I2 ③2KMnO4+16HCl=2KCl+2MnCl2+8H2O+5Cl2↑ (1)若某溶液中有Fe2+、I-和Cl-存在,要除去I-而不影响其他离子的存在,从上述反应物中选出的合适试剂是________。
(2)在强酸性溶液中,将含MnO-4、Fe2+、Fe3+、I-等四种离子的溶液混合,充分反应后:
①若溶液中有I-剩余,则溶液中可能还有上述四种离子中的________,一定无 ________。
②若Fe3+有剩余,则溶液中可能还有上述四种离子中的________,一定无________。
③若Fe2+有剩余,则溶液中可能还有上述四种离子中的________,一定无________。
④若MnO-4剩余,则溶液中可能还有上述四种离子中的________,一定无________。
查看答案和解析>>
科目:高中化学 来源: 题型:022
现有下列三个氧化还原反应:
①2FeCl2+Cl2=2FeCl3 ②2FeCl3+2KI=2FeCl2+2KCl+I2 ③2KMnO4+16HCl=2KCl+2MnCl2+8H2O+5Cl2↑ (1)若某溶液中有Fe2+、I-和Cl-存在,要除去I-而不影响其他离子的存在,从上述反应物中选出的合适试剂是________。
(2)在强酸性溶液中,将含MnO-4、Fe2+、Fe3+、I-等四种离子的溶液混合,充分反应后:
①若溶液中有I-剩余,则溶液中可能还有上述四种离子中的________,一定无 ________。
②若Fe3+有剩余,则溶液中可能还有上述四种离子中的________,一定无________。
③若Fe2+有剩余,则溶液中可能还有上述四种离子中的________,一定无________。
④若MnO-4剩余,则溶液中可能还有上述四种离子中的________,一定无________。
查看答案和解析>>
科目:高中化学 来源:高中化学习题 题型:043
现有下列3个氧化还原反应
①2FeCl3+2KI+2FeCl2+2KI+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+MnCl2+Cl2↑+8H2O
(1)若溶液中有Fe2+、I-和Cl-共存,要除去I-而不影响其他离子的存在,可加入上述反应的试剂是:
[ ]
|
A.Cl2 |
B.KMnO4 |
|
C.FeCl3 |
D.HCl |
(2)在强酸性溶液中,将![]() 、Fe2+、I-、Fe3+四种离子的溶液混合在一起,充分反应后:
、Fe2+、I-、Fe3+四种离子的溶液混合在一起,充分反应后:
①若溶液中有I-剩余,则溶液中一定还有________,一定无________.
②若溶液中有Fe3+剩余,则溶液中可能还有________,一定无________.
③若溶液中有Fe2+剩余,则溶液中可能还有________,一定无________.
④若溶液中有![]() 剩余,则溶液中一定还有________,一定无________.
剩余,则溶液中一定还有________,一定无________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com