
 .E发生银镜反应的离子方程式为
.E发生银镜反应的离子方程式为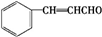 +2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$
+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$ +2Ag↓+3NH3+NN4++H2O.
+2Ag↓+3NH3+NN4++H2O.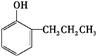 等.
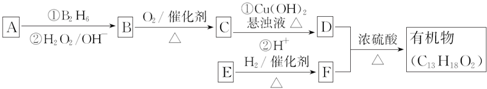
等. 分析 有机物A发生信息中的反应生成B,A应属于烃类,其相对分子质量为56,则$\frac{56}{12}$=4…8,可知A的分子式为C4H8,A的核磁共振氢谱有2组峰且峰面积之比为1:3,B可以连续发生氧化反应,则A为(CH3)2C=CH2,B的结构简式为(CH3)2CHCH2OH,C的结构简式为(CH3)2CHCHO,D的结构简式为(CH3)2CHCOOH,D和F反应生成有机物C13H18O2,应是发生酯化反应,则F为醇,D中含有4个碳原子,所以F中含有9个碳原子,F的分子式为C9H12O,E可以发生银镜反应,含有-CHO,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,可推知E为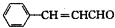 ,F为
,F为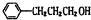 ,则G为
,则G为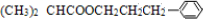 .
.
解答 解:有机物A发生信息中的反应生成B,A应属于烃类,其相对分子质量为56,则$\frac{56}{12}$=4…8,可知A的分子式为C4H8,A的核磁共振氢谱有2组峰且峰面积之比为1:3,B可以连续发生氧化反应,则A为(CH3)2C=CH2,B的结构简式为(CH3)2CHCH2OH,C的结构简式为(CH3)2CHCHO,D的结构简式为(CH3)2CHCOOH,D和F反应生成有机物C13H18O2,应是发生酯化反应,则F为醇,D中含有4个碳原子,所以F中含有9个碳原子,F的分子式为C9H12O,E可以发生银镜反应,含有-CHO,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,可推知E为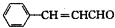 ,F为
,F为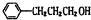 ,则G为
,则G为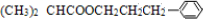 .
.
(1)A为(CH3)2C=CH2,A中所含官能团的名称为碳碳双键,A生成B的反应类型是加成反应,
故答案为:碳碳双键;加成反应;
(2)由上述分析可知,C的结构简式为(CH3)2CHCHO,
故答案为:(CH3)2CHCHO;
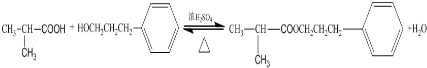
(3)D与F反应是酯化反应,反应方程式为: ,
,
E发生银镜反应的离子方程式为: +2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$
+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$ +2Ag↓+3NH3+NN4++H2O,
+2Ag↓+3NH3+NN4++H2O,
故答案为: ;
; +2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$
+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$ +2Ag↓+3NH3+NN4++H2O;
+2Ag↓+3NH3+NN4++H2O;
(4)F的同分异构体符合:①遇FeCl3溶液显紫色,说明含有酚羟基,②苯环上有两个取代基,F的同分异构体为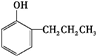 (邻、间、对3种),
(邻、间、对3种),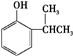 (邻、间、对3种),所以共6种,
(邻、间、对3种),所以共6种,
故答案为:6; 等.
等.
点评 本题考查有机物推断,需要学生对给予的信息进行利用,是常见题型,侧重考查学生的分析推理能力,注意根据相对分子质量与转化关系确定A的结构,熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 100g 30% CH3COOH溶液中含氢原子数为2NA | |
| B. | 标准状况下,11.2 L CCl4中含有C-Cl键的数目为2NA | |
| C. | 16gO3和O2混合物中含氢原子数为NA | |
| D. | 精炼铜过程中阳极质量减少6.4g时,电路中转移电子数等于0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
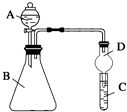 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试验编号 | 温度(℃) | 催化剂用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响 b.实验1和3探究反应物浓度对该反应速率的影响. c.实验2和4探究催化剂对反应速率的影响 | |
| 体积(mL) | 浓度(mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |

| 试验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
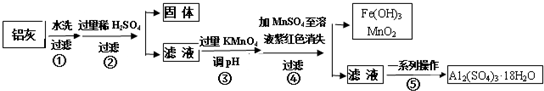
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
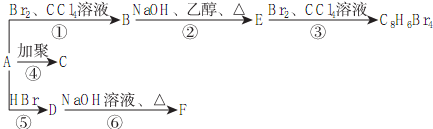
 ,D
,D ,E
,E .
.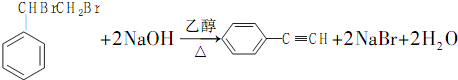 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 沸点/℃ | 物质 | 沸点/℃ |
| 溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
| 苯甲醛 | 179 | 间溴苯甲醛 | 229 |
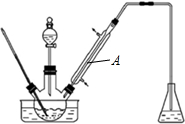
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com