
| A.c(NH4+)>c(Cl-),c(OH-)>c(H+) |
| B.c(Cl-)>c(NH4+),c(H+)>c(OH-) |
| C.c(NH4+)=c(Cl-),c(OH-)=c(H+) |
| D.c(Cl-)>c(NH4+),c(OH-)>c(H+) |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeCl2、FeCl3 | B.NaHCO3、Na2CO3 |
| C.Al2(SO4)3、AlCl3 | D.NH4HCO3、NH4Cl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.常温下PH=2的甲酸与pH=12的烧碱溶液等体积混合: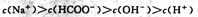 |
B.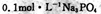 溶液中: 溶液中: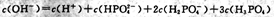 |
C.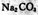 溶液加水稀释后,恢复至原温度,所有离子浓度均减小 溶液加水稀释后,恢复至原温度,所有离子浓度均减小 |
| D. 1L 0.3mol ?L-1NaOH溶液吸收标准状况下4. 48L CO2: |
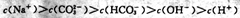
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在Na3PO4溶液中,c(Na+)是c(PO43-)的3倍 |
| B.pH为3的盐酸中,其c(H+)是pH为1的盐酸中c(H+)的3倍 |
| C.0.1 mol·L-1KOH溶液和0.1 mol·L-1氨水中,其c(OH-)相等 |
| D.在25℃时,无论是酸性、碱性还是中性的稀溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
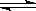 Mg2++2OH-,NH4++OH-
Mg2++2OH-,NH4++OH-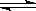 NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释 。
NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
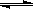 Fe(OH)3+3HCl若要使FeCl3的水解程
Fe(OH)3+3HCl若要使FeCl3的水解程 度增大,应采取的方法是
度增大,应采取的方法是| A.加入NaHCO3 | B.加入AgNO3 | C.加FeCl3固体 | D.加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com