

科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 实验序号 | a | b | c |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.005 mol |
| B.0.010 mol |
| C.0.020 mol |
| D.0.030 mol |
查看答案和解析>>
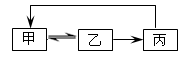
科目:高中化学 来源:不详 题型:单选题
| | 甲 | 乙 | 丙 |
| A | CH2=CH2 | CH3CH2Cl | CH3CH2OH |
| B | SiO2 | H2SiO3 | Na2SiO3 |
| C | Cl2 | HCl | CuCl2 |
| D | AlCl3 | Al(OH)3 | Al2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.利用铝与氧化铁发生的铝热反应来焊接钢轨 |
| B.向某种消毒液( NaC1O)中滴加醋酸,能抑制NaC1O水解,降低漂白效果 |
| C.医用双氧水涂抹伤口时,有气泡产生,这是由溶解在血液中的O2、CO2逸出形成的 |
| D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验探究内容 | 实验用品 |
| A | 铜丝在氯气中燃烧 | 坩埚钳、燃烧匙、氯气、铜丝 |
| B | 铝热反应 | 铁架台、大蒸发皿、普通漏斗、铝粉、Fe2O3 |
| C | 实验室制备氨气 | 试管、集气瓶、酒精灯、NH4Cl、Ca(OH)2 |
| D | 用KMnO4晶体配制500mL0.1mol·L-1KMnO4溶液 | 容量瓶、烧杯、玻璃棒、酸式滴定管、KMnO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com