
| 18g |
| 18g/mol |
| 26.4g |
| 44g/mol |
| 0.8mol |
| 0.2mol |
| 2mol |
| 0.2mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Na+、Cl-、SO42- |
| B、Ag+、Al3+、NO3-、H+ |
| C、Na+、HCO3-、Cl-、OH- |
| D、K+、H+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素X形成的单质一定是原子晶体 |
| B、原子半径的大小顺序:r(W)>r(Z)>r(Y)>r (X) |
| C、Y与氧元素形成的化合物Y2O2中阴、阳离子的个数比为1:2 |
| D、W分别与Y、Z形成的化合物中含有的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
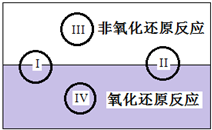 氧化还原反应在生产、生活中具有广泛的用途.
氧化还原反应在生产、生活中具有广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
| O | 2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.
2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | |||||||||||||||||
| ③ | ④ | ⑤ | |||||||||||||||
| ② | ⑥ | ||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①>②>④>③ |
| B、②>③>④>① |
| C、①>②>③>④ |
| D、③>②>④>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com