
下列说法正确的是( )
A.等质量的乙烯和丙烯中,所含碳原子数之比为2∶3
B.等体积、等浓度的NH4Cl溶液和稀氨水中,所含NH4+的数目相等
C.等物质的量的过氧化钡(BaO2)和Ba(OH)2固体中,阴阳离子个数比均为2∶1
D.等物质的量的Cl2分别与足量的Fe和Cu反应,转移的电子数相等
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:
v(H2O2)≈3.3×10-2mol·L-1·min-1
B.0~6 min的平均反应速率:
v(H2O2)<3.3×10-2mol·L-1·min-1
C.反应至6 min时,c(H2O2)=0.30 mol/L
D.反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断不正确的是( )
A.沸点:NH3>PH3>AsH3 B. 熔点:Si3N4>NaCl>SiI4
C.酸性:HClO4>H2SO4>H3PO4 D. 碱性:NaOH>Mg(OH)2>Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | Li在氧气中燃烧主要生成Li2O2 |
|
| B. | 将SO2通入BaCl2溶液可生成BaSO3沉淀 |
|
| C. | 将CO2通入次氯酸钙溶液可生成次氯酸 |
|
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在制定溶液中一定能大量共存的是 ( )
A.澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl-
B.c(Fe3+)=0.1mol·Lˉ1的溶液中:Na+、NH4+、SCN-、SO42-
C.加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3-
D.0.1mol·Lˉ1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一。对下列反应的推断或解释正确的是 ( )
| 操作 | 可能的实验现象 | 解释 | |
| A | 某溶液中加入硝酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO |
| B | 向CaSO3中加入硝酸 | 有刺激性气味的气体生成 | CaSO3与硝酸反应生成SO2 |
| C | 同温同压下用pH试纸测定相同浓度的碳酸钠和硫酸钠溶液的酸碱性 | 碳酸钠溶液显碱性,硫酸钠溶液显中性 | 碳酸钠溶液发生了水解 |
| D | 向淀粉KI溶液中通入Cl2 | 溶液变蓝 | Cl2与淀粉发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
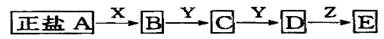 |
当X是强酸时,A、B、C、D、E均含有同一种元素;当X是强碱时,A、B、C、D、E均含有另一种元素
回答下列问题(用化学式填写):
(1)A是________________,Y是_______________,Z是________________.
(2)当X是强碱时,E是________________.
(3)当X是强酸时,E是________________.
(4)写出A与X(是强酸时)反应的离子方程式__________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3,若将X通入澄清石灰水中,无沉淀产生,则有关气体X的成分的下列说法正确的是( )
①一定含有HBr,可能含有CO2 ②一定不含CO2 ③一定不含NH3、Cl2 ④可能含有Cl2、CO2.
|
| A. | 只有① | B. | 只有③ | C. | ①和③ | D. | ②和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是
A.离子键没有方向性和饱和性,而共价键有方向性和饱和性
B.离子键的强弱主要决定于离子半径和离子所带电荷数
C.配位键在形成时,由成键双方各提供一个电子形成一对共用电子
D.金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com