
下表是五种银盐的溶度积常数(25 ℃),下列有关说法错误的是( )
化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.5×10-16 |
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将AgCl溶解于水后,向其中加入Na2S,则可以生成黑色的Ag2S沉淀
C.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
D.常温下,AgCl、AgBr和AgI三种物质的溶解度逐渐增大
 考前必练系列答案
考前必练系列答案科目:高中化学 来源:2015-2016学年山西省太原市高一下学期期末化学试卷(解析版) 题型:简答题
海洋具有十分巨大的开发潜力,人民可以从海水中获得多种物质。
(1)不需经过化学变化就能从海水中获得的一种物质是________________________
(2)经上述操作后剩余的浓缩海水中含有大量的Mg2+,从中提取金属镁的流程如下:
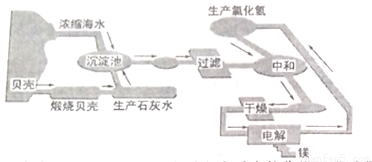
①贝壳的主要成分是CaCO3,燃烧贝壳时发生反应的化学方程式是____________________________;在沉淀中生成的Mg(OH)2的离子方程式是________________________。
②过滤后向Mg(OH)2中加入________________即得到MgCl2溶液,在经过一系列操作得到MgCl2。
③电解熔融MgCl2得到镁蒸气,同时生成___________ ________________,它可用于上述流程中的_____________________________步骤,这样做的好处是__________________________,镁蒸气冷却后即为固体镁,冷却镁蒸气时可在下列哪种气体氛围中进行__________(填序号)
A.H2 B.O2 C.空气
④上述与含镁物质有关的操作中,消耗能量最多的步骤是_____________,原因是_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄香、航天等校高一下学期期末联化学试卷(解析版) 题型:选择题
一定条件下,在容积为5 L密闭容器中发生反应:2SO2(g)+ O2(g) 2SO3(g),半分钟后测得生成0.04molSO3。在这段时间内O2的化学反应速率为( )
2SO3(g),半分钟后测得生成0.04molSO3。在这段时间内O2的化学反应速率为( )
A.0.004(mol•L?1•min?1)
B.0.008(mol•L?1•min?1)
C.0.016(mol•L?1•min?1)
D.0.032(mol•L?1•min?1)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄香、航天等校高二下学期期末联化学试卷(解析版) 题型:选择题
某化合物6.4g在氧气中完全燃烧,只生成8.8g CO2和7.2 g H2O。下列说法正确的是( )
A. 该化合物仅含碳、氢两种元素
B. 该化合物一定是C2H8O2
C. 无法确定该化合物是否含有氧元素
D. 该化合物中碳、氢原子个数比为1:4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄香、航天等校高二下学期期末联化学试卷(解析版) 题型:选择题
用VSEPR模型预测下列分子或离子的立体结构,其中不正确的是( )
A.NH4+为正四面体形
B.CS2为直线形
C.HCN为折线形(V形)
D.PCl3为三角锥形
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄香、航天等校高二下学期期末联化学试卷(解析版) 题型:选择题
如图所示:甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )
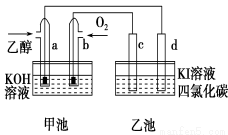
A.两个装置之间没有盐桥,故不能形成电流
B.一段时间后,乙池d电极周围的溶液呈现棕褐色
C.a电极的电极反应式C2H5OH+16OH--12e-=2CO32-+11H2O
D.乙池在反应前后溶液的pH不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省漳州市高二下期末化学试卷(解析版) 题型:选择题
下列文字表述与反应方程式对应且正确的是( )
A.乙醇与溴化氢的水溶液共热:CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
B.甲烷和氯气在光照条件下的反应:2CH4+Cl2 2CH3Cl+H2
2CH3Cl+H2
C.苯酚溶液中滴入NaOH溶液:H+ + OH- H2O
H2O
D.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32—
2C6H5OH + 2CO32—
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一下学期期末化学试卷(解析版) 题型:填空题
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为________,氧化性最弱的简单阳离子是________。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是_______________________________ ___;
制铝时,电解Al2O3而不电解AlCl3的原因是____________________________ __。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料,SiCl4(熔点-70 ℃)。由粗硅制纯硅过程如下:
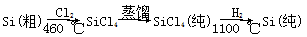
SiCl4属于 晶体。在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:______________________________________ 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是________。
a.NH3b.HI c.SO2d.CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下学期期末化学试卷(解析版) 题型:选择题
某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为( )
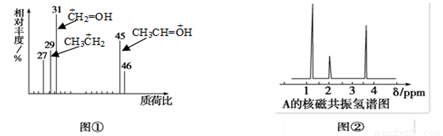
A. HCOOH B. CH3CHO C. CH3CH2OH D. CH3CH2CH2COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com