
【题目】已知某强酸性溶液中存在较多的Ba2+、NO3-,则溶液中还可能大量存在的离子组是
A.K+、NH4+、HCO3- B.Na+、Cu2+、Cl-
C.Cu2+、Mg2+、SO42- D.Fe2+、Ca2+、Cl-
 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( )
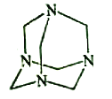
A.1:1 B.2:3 C.3:2 D.2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaClO3和NaI按物质的量之比1:1混合于烧瓶中,滴入适量硫酸,并水浴加热,反应后测得NaClO3和NaI恰好完全反应,生成I2、Na2SO4和H2O,并产生棕黄色的气体X,则X为
A.Cl2 B.Cl2O C.ClO2 D.Cl2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
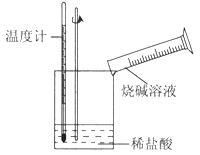
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是__________(填“吸热”或“放热”)反应,其离子方程式是_________________________。
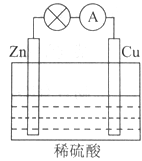
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。原电池工作一段时间后,若消耗锌6.5g,则放出标准状况下气体__________L,电路中通过的电子数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(如图所示)在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡。在另一支试管中加入饱和碳酸钠溶液用来吸收反应生成物。
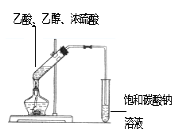
小心均匀加热大试管3-5min.请回答问题:
(1)在大试管中的反应化学方程式: ,
反应类型为_________________。
(2)用来吸收反应生成物的试管里要装饱和碳酸钠溶液的原因是: 。
(3)出气导管口不能插入碳酸钠液面的原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6是一种优良的绝缘气体,分子结构中存在S-F键.已知1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F、S-F键需吸收的能量分别为160kJ、330kJ。则发生反应S(s)+3F2(g)═SF6(g),生成1molSF6时能量变化为( )
A、释放1220KJ B、吸收1780KJ C、 吸收1220KJ D、释放1780KJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com