
【题目】常温下,有pH为12的NaOH溶液100mL.
(1)此溶液中水电离出的氢离子浓度c(H+)为 .
(2)若将该溶液的pH变为11(设混合后溶液体积不变). ①若用蒸馏水稀释,应加入 mL.
②若用pH=10的NaOH溶液稀释,应加入 mL.
【答案】
(1)1.0×10﹣12mol?L﹣1
(2)900;1000
【解析】解答:(1)常温下pH=12的氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子为水电离的,则水电离的氢离子浓度为:c(H+)=1.0×10﹣12molL﹣1 , 所以答案为:1.0×10﹣12molL﹣1;(2)①常温下pH=12的氢氧化钠溶液中,氢氧根离子浓度为:0.01mol/L,pH=11的溶液中氢氧根离子浓度为0.001mol/L,稀释过程中溶质的物质的量不变,则稀释后溶液体积为: ![]() =11L=1000mL,需要加入的蒸馏水体积为:1000mL﹣100mL=900mL, 所以答案为:900;②pH=10的氢氧化钠溶液中氢氧根离子浓度为0.0001mol/L,设加入pH=10的氢氧化钠溶液体积为V,则:
=11L=1000mL,需要加入的蒸馏水体积为:1000mL﹣100mL=900mL, 所以答案为:900;②pH=10的氢氧化钠溶液中氢氧根离子浓度为0.0001mol/L,设加入pH=10的氢氧化钠溶液体积为V,则: ![]() =0.001mol/L,解得:V=1L=1000mL,
=0.001mol/L,解得:V=1L=1000mL,
所以答案为:1000.
分析:本题考查了溶液pH的简单计算、水的电离及其影响,注意明确酸碱溶液抑制了水的电离,熟练掌握溶液酸碱性与溶液pH的关系及计算方法.


科目:高中化学 来源: 题型:
【题目】下列各项操作,有错误的是( )
A. 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B. 进行分液时,分液漏斗中的下层液体,从下端流出,上层液体则从上口倒出
C. 萃取、分液前需对分液漏斗检漏
D. 为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于药物的使用说法正确的是( )
A.因碘酒使蛋白质变性,故常用于外用消毒
B.使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验
C.长期大量使用阿司匹林可预防疾病,没有副作用
D.能用于治疗胃酸过多的抗酸药通常含有麻黄碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示:
(1)25℃时,将pH=3 的H2SO4溶液与pH=10的NaOH溶液混合,若所得混合溶液的pH=7,则H2SO4溶液与NaOH溶液的体积比为 .
(2)T℃时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
(3)曲线B对应温度下,pH=3的HCl溶液和pH=9的某碱溶液等体积混合后,混合溶液的pH=7.请分析其原因: . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.23 g金属钠投入到100 ml水中,使其充分反应,假设反应后溶液的体积不变。试计算:
(1)反应后所得溶液溶质的物质的量浓度是多少?
(2)产生标准状况下的气体多少毫升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置中能达到实验目的是( ) 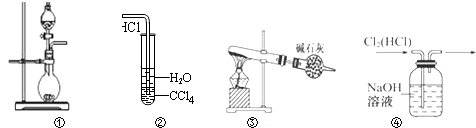
A.图①可用于制取少量NH3或用MnO2和浓盐酸制取Cl2
B.装置②可用于氯化氢气体溶于水
C.以NH4Cl为原料,装置③可用于实验室制备少量干燥的NH3
D.装置④可用于除去Cl2中的HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com