
 .
. (写出结构简式).
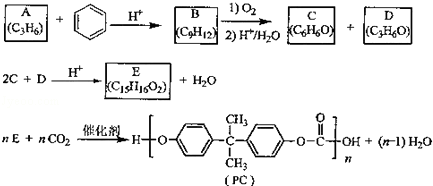
(写出结构简式).分析 A可使溴的CCl4溶液褪色,故A(C3H6)是丙烯(CH3-CH=CH2),B中有五种不同化学环境的氢说明B中有五种等效氢原子,又根据B的分子式C9H12,可推知B为 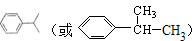 ,C(C6H6O)可与FeCl3的溶液发生显色反应,可知C为
,C(C6H6O)可与FeCl3的溶液发生显色反应,可知C为 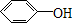 ,D不能使溴的CCl4溶液褪色,其核磁共振氢谱为单峰,说明D中只有一种等效氢原子,则D为丙酮(
,D不能使溴的CCl4溶液褪色,其核磁共振氢谱为单峰,说明D中只有一种等效氢原子,则D为丙酮(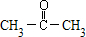 ),故可写出C与D反应生成E的化学方程式为
),故可写出C与D反应生成E的化学方程式为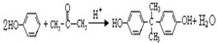 ,B(C9H12)有多种同分异构体,含有一个取代基时(B除外)有CH2CH2CH3,两个取代基:甲基和乙基在苯环上出现邻、间、对三种结构,三个相同的取代基(三个甲基)有连、偏、均三种形式,即
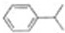
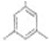
,B(C9H12)有多种同分异构体,含有一个取代基时(B除外)有CH2CH2CH3,两个取代基:甲基和乙基在苯环上出现邻、间、对三种结构,三个相同的取代基(三个甲基)有连、偏、均三种形式,即 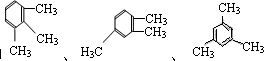 .故含苯环的共有7种;其中在核磁共振氢谱中出现两组峰,且面积之比为3:1的是
.故含苯环的共有7种;其中在核磁共振氢谱中出现两组峰,且面积之比为3:1的是 ,据此答题.
,据此答题.
解答 解:A可使溴的CCl4溶液褪色,故A(C3H6)是丙烯(CH3-CH=CH2),B中有五种不同化学环境的氢说明B中有五种等效氢原子,又根据B的分子式C9H12,可推知B为  ,C(C6H6O)可与FeCl3的溶液发生显色反应,可知C为
,C(C6H6O)可与FeCl3的溶液发生显色反应,可知C为  ,D不能使溴的CCl4溶液褪色,其核磁共振氢谱为单峰,说明D中只有一种等效氢原子,则D为丙酮(
,D不能使溴的CCl4溶液褪色,其核磁共振氢谱为单峰,说明D中只有一种等效氢原子,则D为丙酮(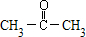 ),故可写出C与D反应生成E的化学方程式为
),故可写出C与D反应生成E的化学方程式为 ,
,
(1)根据上面的分析可知,A(C3H6)是丙烯(CH3-CH=CH2),故答案为:丙烯;
(2)依据题给信息可知:E与CO2反应生成PC的反应类型为缩聚反应,故答案为:缩聚反应;
(3)根据上面的分析可知,B为  ,故答案为:
,故答案为: ;
;
(4)B(C9H12)有多种同分异构体,含有一个取代基时(B除外)有-CH2CH2CH3,两个取代基:甲基和乙基在苯环上出现邻、间、对三种结构,三个相同的取代基(三个甲基)有连、偏、均三种形式,即  ,故含苯环的共有7种;其中在核磁共振氢谱中出现两组峰,且面积之比为3:1的是
,故含苯环的共有7种;其中在核磁共振氢谱中出现两组峰,且面积之比为3:1的是 ,故答案为:7;
,故答案为:7; ;
;
(5)分子式为C9H10O2的芳香族化合物,属于酯类且只有一个侧链,符合条件的同分异构体有: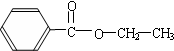 ,
,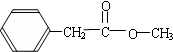 ,
,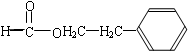 ,
,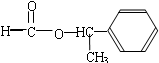 ,
,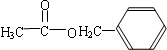 ,
,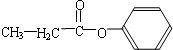 ,
,
故答案为:6;
(6)D为丙酮(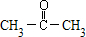 ),D物质可经五步反应制备丙三醇,丙酮与氢气加成反应生成2-丙醇,2-丙醇在浓硫酸作用下发生消去反应生成丙烯,依据题给已知条件:CH2=CH-CH3+Cl2$\stackrel{500℃}{→}$ CH2=CH-CH2Cl+HCl,丙烯与氯气在500℃下生成CH2=CH-CH2Cl,然后洗物质与氯气加成,最后再氢氧化钠水溶液中水解即可得到,
),D物质可经五步反应制备丙三醇,丙酮与氢气加成反应生成2-丙醇,2-丙醇在浓硫酸作用下发生消去反应生成丙烯,依据题给已知条件:CH2=CH-CH3+Cl2$\stackrel{500℃}{→}$ CH2=CH-CH2Cl+HCl,丙烯与氯气在500℃下生成CH2=CH-CH2Cl,然后洗物质与氯气加成,最后再氢氧化钠水溶液中水解即可得到,
对应的各步方程式为:
第一步:CH3COCH3+H2$\stackrel{催化剂}{→}$CH3CHOHCH3;
第二步:CH3CHOHCH3 $→_{△}^{浓硫酸}$CH3CH=CH2+H2O;
第三步:CH2=CH-CH3+Cl2$\stackrel{500℃}{→}$ CH2=CH-CH2Cl+HCl;
第四步:CH2=CH-CH2Cl+Cl2→CH2Cl-CHCl-CH2Cl;
第五步:CH2Cl-CHCl-CH2Cl+3NaOH$→_{△}^{水}$ CH2COH-CHOH-CH2OH+3NaCl,
故答案为:CH3COCH3+H2$\stackrel{催化剂}{→}$CH3CHOHCH3;CH3CHOHCH3 $→_{△}^{浓硫酸}$CH3CH=CH2+H2O;CH2=CH-CH3+Cl2$\stackrel{500℃}{→}$ CH2=CH-CH2Cl+HCl;CH2=CH-CH2Cl+Cl2→CH2Cl-CHCl-CH2Cl;CH2Cl-CHCl-CH2Cl+3NaOH$→_{△}^{水}$ CH2COH-CHOH-CH2OH+3NaCl.
点评 本题考查有机物推断、有机物命名、官能团、同分异构体等,注意根据反应条件及分子式进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应的发生均无需加热 | |
| B. | 凡是需要加热后才能发生的反应一定是吸热反应 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 物质发生化学反应都伴随着能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C三种元素形成的化合物一定是非电解质 | |
| B. | A与C只能形成化学式为A2C的化合物 | |
| C. | 第三周期中,D的原子半径最大 | |
| D. | E的氧化物对应的水化物一定具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
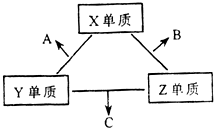 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: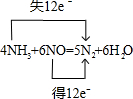
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
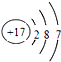 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
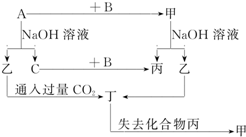 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCHO CH3COOH | B. | HCOOCH3 CH3COOH | ||
| C. | C2H4 C2H5OH | D. | CH3OH C10H8O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com