
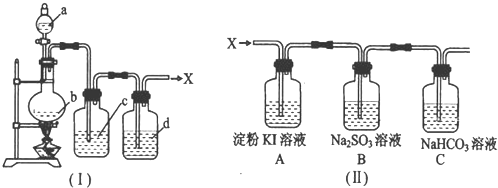
浓盐酸与重铬酸钾[K2Cr2O7(s)]共热时产生某种气体单质X,产物中还有三氯化铬等生成。这种方法制X时便于控制反应,撤去酒精灯则反应停止。现在要制得纯净的X(装置如图)。

(1)加热时,a与b反应的化学方程式__________________________________
(2)液体C的作用是_____________________________________________
现在把制得的纯净干燥的X通入下图所示的装置。

(3)e是FeBr2溶液,一段时间后观察到的实验现X象是________________________________
(4)f是浸有一种钾盐溶液的棉球,一段时同后观察到试管内有紫色气体,则大试管内发生反应的化学方程式为________________________
(5)g是水和CCl4的混合物,可看到颜色较深的液体在____ (填“上”或“下”)层.
(6)h是碱石灰,则此装置的作用是______________________________________________
(1)14HCl(浓)+K2Cr2O7![]() 2KCl+2CrCl3+3Cl2↑+7H2O(3分)
2KCl+2CrCl3+3Cl2↑+7H2O(3分)
(2)除HCl(1分)
(3)溶液由浅绿色变成黄色,再变成棕黄色(2分)
(4) Cl2+2KI=I2+2KCl(2分)
(5)下(1分)
(6)吸收多余的Cl2(1分)
本题由信息可以知道加热时,a与b反应的化学方程式14HCl(浓)+K2Cr2O7![]() 2KCl+2CrCl3+3Cl2↑+7H2O,要得到纯净干燥的Cl2先除去HCl和H20,所以C为饱和食盐水除去HCl,D为浓硫酸除去H20。Cl2有强氧化性,和FeBr2反应,反应先后规律:当有多种氧化剂、多种还原剂时,氧化性越强的氧化剂、还原性越强的还原剂越先反应。如:FeBr2和Cl2反应时,由于Fe2+离子的还原性比Br-离子的还原性强,所以Cl2先氧化Fe2+离子,Cl2过量时再氧化Br-离子。因此, FeBr2和少量Cl2反应时,离子方程式是:2 Fe2++ Cl2=2 Fe3++2Cl-; FeBr2和过量Cl2反应时,离子方程式是:2Fe2++4Br-+3Cl2-=2Fe3++2Br2+6Cl-。现象为溶液由浅绿色变成黄色,再变成棕黄色。由f是浸有一种钾盐溶液的棉球,一段时同后观察到试管内有紫色气体,马上就确定Cl2+2KI=I2+2KCl。g是水和CCl4的混合物,I2在里面分层,CCl4比水的密度大,在下层。h是碱石灰吸收多余的Cl2。
2KCl+2CrCl3+3Cl2↑+7H2O,要得到纯净干燥的Cl2先除去HCl和H20,所以C为饱和食盐水除去HCl,D为浓硫酸除去H20。Cl2有强氧化性,和FeBr2反应,反应先后规律:当有多种氧化剂、多种还原剂时,氧化性越强的氧化剂、还原性越强的还原剂越先反应。如:FeBr2和Cl2反应时,由于Fe2+离子的还原性比Br-离子的还原性强,所以Cl2先氧化Fe2+离子,Cl2过量时再氧化Br-离子。因此, FeBr2和少量Cl2反应时,离子方程式是:2 Fe2++ Cl2=2 Fe3++2Cl-; FeBr2和过量Cl2反应时,离子方程式是:2Fe2++4Br-+3Cl2-=2Fe3++2Br2+6Cl-。现象为溶液由浅绿色变成黄色,再变成棕黄色。由f是浸有一种钾盐溶液的棉球,一段时同后观察到试管内有紫色气体,马上就确定Cl2+2KI=I2+2KCl。g是水和CCl4的混合物,I2在里面分层,CCl4比水的密度大,在下层。h是碱石灰吸收多余的Cl2。


科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022

(1)完成并配平下列反应方程式:
( )![]() +( )HCl——(
)
+( )HCl——(
)![]() +( )+( )+( )
+( )+( )+( )
(2)要得到纯净的X气体,A瓶应盛________,B瓶应盛________.
(3)在C处的白色晶体是________,D瓶内紫黑色的晶体是________;在C处加热的目的是________.
(4)E管应连接________装置,原因是_______________________________.
(5)有位同学想循环利用从D瓶出来的X气体,为此他从D瓶连接一根导管F到B瓶,你认为行吗?(说明原因)
______________________________________________________.
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:058
在下图所示的装置中,当浓盐酸与重铬酸钾(K2Cr2O7)共热时产生气体单质X,X经A和B两洗气瓶后在C处与热的白色晶体反应,最后在D瓶底部有黑色晶状物.

请回答下列问题:
(1)制取X气体需用到的玻璃仪器有________.
(2)检验X气体,可用________.
(3)要得到纯净的X气体,A瓶盛________,作用是________;B瓶盛________,作用是________.
(4)C处白色晶体是________,D瓶底的晶状物是________.
(5)在C处加热的目的是________.
(6)E装置内盛的是碱石灰,其作用是________.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058

(1)加热时在a中的浓盐酸与重铬酸钾反应的化学方程式是________。
(2)液体c应使用什么试剂(写化学式表示溶质)________,其作用是________。
(3)液体d应是________________,其作用是________。现把制得的纯净干燥的X通入下图所示装置:在锥形瓶f里有紫黑色具金属光泽的晶体沉积。
(4)e中放入的白色钾盐________,反应时的化学方程式是________。

(5)g中盛有碱石灰它有两重作用是:
①________________________________________;
②________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com