
��8�֣��� ������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺
��д��������Ӧ�����ӷ���ʽ________________________________��
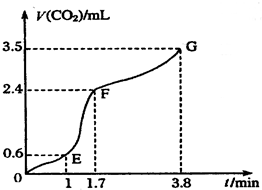
��ʵ������л��Ƴ�����CO2�����[V��CO2��]��ʱ�䣨t���Ĺ�ϵ��ͼ��ʾ���Է����ж�OE�Ρ�EF�Ρ�FG�η�Ӧ���ʣ��ֱ���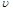 ��OE����
��OE����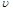 ��EF����
��EF����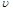 ��FG����ʾ���ĸ����______________��
��FG����ʾ���ĸ����______________��

�Ƚ�OE�κ�EF�Σ�˵��EF�����ʱ仯����Ҫԭ�������______________ ____
�� ��ӦA + 3B = 2C + 2D�������ֲ�ͬ������µķ�Ӧ���ʷֱ�Ϊ��
�٦�(A)��0.15mol/(L��s) �ڦ�(B)��0.6mol/(L��s)
�ۦ�(C)��0.4mol/(L��s) �ܦ�(D)��0.45mol/(L��s)
�÷�Ӧ���еĿ���˳��Ϊ__ ��
��8�֣�
���CaCO3+2H+��Ca2++H2O+CO2������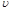 ��EF�����¶Ƚϸߡ�Ũ�Ƚϴ�
��EF�����¶Ƚϸߡ�Ũ�Ƚϴ�
�� �ܣ��ڣ��ۣ���
��������I:��Ӧ������ָ��λʱ�������ʵ����ĸı�ֵ����ͼ���ǵ�Ȼ��б�ʴ�ĵط����ʴ�������Ҫ�����ڷ�Ӧ��ı��ԣ���Ҳ��������¶ȡ�Ũ�ȵȵ�Ӱ�졣����Ӧ��ʼ��EF�ε�����ȴ���˵����Ӧ��Ũ�Ƚϴ�����Ҫ�Ļ��Ƿ�Ӧ�ų����������¡�
II:���ĸ������Է���ʽϵ����Ϊ��ת��Ϊͬһ���ʵ������ٽ��бȽϡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺
��������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣��� ������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺
��д��������Ӧ�����ӷ���ʽ________________________________��
��ʵ������л��Ƴ�����CO2�����[V��CO2��]��ʱ�䣨t���Ĺ�ϵ��ͼ��ʾ���Է����ж�OE�Ρ�EF�Ρ�FG�η�Ӧ���ʣ��ֱ��� ��OE����
��OE����![]() ��EF����
��EF����![]() ��FG����ʾ���ĸ����______________��
��FG����ʾ���ĸ����______________��
�Ƚ�OE�κ�EF�Σ�˵��EF�����ʱ仯����Ҫԭ�������______________ ____
�� ��ӦA + 3B = 2C + 2D�������ֲ�ͬ������µķ�Ӧ���ʷֱ�Ϊ��
�٦�(A)��0.15mol/(L��s) �ڦ�(B)��0.6mol/(L��s)
�ۦ�(C)��0.4mol/(L��s) �ܦ�(D)��0.45mol/(L��s)
�÷�Ӧ���еĿ���˳��Ϊ__ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ̩����ѧ��һ��ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��8�֣��� ������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺
��д��������Ӧ�����ӷ���ʽ________________________________��
��ʵ������л��Ƴ�����CO2�����[V��CO2��]��ʱ�䣨t���Ĺ�ϵ��ͼ��ʾ���Է����ж�OE�Ρ�EF�Ρ�FG�η�Ӧ���ʣ��ֱ��� ��OE����
��OE���� ��EF����
��EF���� ��FG����ʾ���ĸ����______________��
��FG����ʾ���ĸ����______________��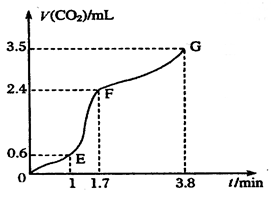
�Ƚ�OE�κ�EF�Σ�˵��EF�����ʱ仯����Ҫԭ�������______________ ____
�� ��ӦA + 3B =" 2C" + 2D�������ֲ�ͬ������µķ�Ӧ���ʷֱ�Ϊ��
�٦�(A)��0.15mol/(L��s) �ڦ�(B)��0.6mol/(L��s)
�ۦ�(C)��0.4mol/(L��s) �ܦ�(D)��0.45mol/(L��s)
�÷�Ӧ���еĿ���˳��Ϊ__ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
I. ʵ�������ö������̺�Ũ���������ȡ�������÷�Ӧ�����ӷ���ʽΪ�� MnO2+4H++2Cl��![]() Mn2++Cl2��+2H2O��Ҳ�������÷�Ӧ��
Mn2++Cl2��+2H2O��Ҳ�������÷�Ӧ��
2KMnO4+16HCl��Ũ�� 2KCl+2MnCl2+5Cl2��+8H2O��ȡ���ռ����������������������װ����ͼ��ʾ��
|
��1������KMnO4��Ũ����Ϊԭ����ȡ����������ݷ�Ӧԭ������ͼ��ѡ����ʵ�����װ�� ������ţ���
|
��2��װ��B�������� ��
��3��E�е��Լ���ѡ�� ������ţ���
A��NaOH��Һ B��Na2CO3��Һ C��NaCl��Һ D��ˮ
��4��ijѧ��ͨ���������ַ�ʽ��ȡ������
����8.7gMnO2������Ũ���ᷴӦ��ȡCl2
���ú�14.6gHCl��Ũ����������MnO2��Ӧ��ȡCl2
�����ַ�ʽ����Cl2�����Ĺ�ϵ�� ��
A���ٶ� B���ڶ� C���٢�һ����
II��������̼��ƹ����ϡ���ᷴӦ��ȡCO2���壬��ش��������⣺
��1��д��������Ӧ�����ӷ���ʽ ��
|
[V��CO2��]��ʱ�䣨t���Ĺ�ϵ��ͼ
��ʾ���Է����ж�OE�Ρ�EF�Ρ�
FG�η�Ӧ����[�ֱ���![]() ��OE����
��OE����![]()
��EF����![]() ��FG����ʾ]�Ĵ�С��ϵ
��FG����ʾ]�Ĵ�С��ϵ
���Ƚ�OE�κ�EF
�Σ�˵��EF�����ʱ仯����Ҫԭ��
Ӧ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com