
| A. | 2:1:2 | B. | 5:5:4 | C. | 1:1:1 | D. | 无法确定 |
分析 设出烧瓶体积,根据n=$\frac{V}{{V}_{m}}$计算出烧瓶中气体的物质的量,干燥、纯净的NH3中溶液充满烧瓶,含一半空气的氯化氢气体形成的溶液体积为烧瓶容积的一半,根据c=$\frac{n}{V}$计算出溶液的浓度;根据反应4NO2+O2+2H2O=4HNO3计算出反应后溶质的物质的量,再根据c=$\frac{n}{V}$计算出硝酸的浓度,最后计算出三个烧瓶中所得溶液的物质的量浓度之比.
解答 解:假设烧瓶体积为5VL,则干燥纯净的氨气体积为5VL完全溶于水后烧瓶充满溶液溶液体积也是5VL,溶质物质的量浓度为:$\frac{\frac{5VL}{22.4L/mol}}{5VL}$=$\frac{1}{22.4}$mol/L;
含一半空气的氯化氢烧瓶中氯化氢体积为2.5V完全溶解后烧瓶进水$\frac{1}{2}$,也就是溶液体积为2.5V,所以溶质物质的量浓度为:$\frac{\frac{2.5VL}{22.4L/mol}}{2.5VL}$=$\frac{1}{22.4}$mol/L;
二氧化氮与氧气体积比为4:1的混合气中NO2体积为4VL,根据以下方程式恰好完全反应:4NO2+O2+2H2O=4HNO3,而且生成硝酸物质的量为:$\frac{4VL}{22.4L/mol}$=$\frac{4V}{22.4}$mol,
由于完全反应所以烧瓶充满溶液其体积为5VL,所以溶质的物质的量浓度为:$\frac{\frac{4V}{22.4}mol}{5V}$=$\frac{1}{28}$mol/L,
所以三个烧瓶中所得溶液的溶质的物质的量浓度之比为:=$\frac{1}{22.4}$mol/L:=$\frac{1}{22.4}$mol/L:$\frac{1}{28}$mol/L=5:5:4,
故选B.
点评 本题考查物质的量浓度的计算,题目难度中等,解答时要把握二氧化氮与水反应的性质,然后根据物质的量浓度的计算公式进行计算.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
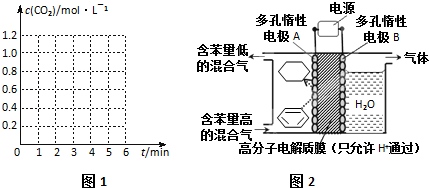
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
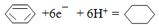 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②③ | C. | ②④ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,33.6 L 氟化氢中含有氟原子的数目为1.5NA | |
| B. | pH均为5的NH4Cl和NaHSO4溶液中水电离出的氢离子数目均为10-5NA | |
| C. | 在1L 0.1 mol•L-1CuSO4溶液中,阴离子总数大于0.1 NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molIH2,在一定条件下充分反应,转移电子的数目为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其水溶液显酸性,俗称石碳酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后立即放出二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | C | |
| B |
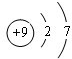 ,比较B、C的原子半径:B>C;
,比较B、C的原子半径:B>C;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com