
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.c(Fe3+)=0.1mol/L 的溶液:![]() 、Na+、Cl、
、Na+、Cl、![]()
B.碱性溶液中:Al3+、Fe3+、![]() 、
、![]()
C.水电离出的c(H+)=1×1012mol/L的溶液:![]() 、
、![]() 、
、![]() 、Cl
、Cl
D.pH =12的溶液中:Na+、![]() Cl、
Cl、![]()
科目:高中化学 来源: 题型:
【题目】几种有机物的相互转化如图:
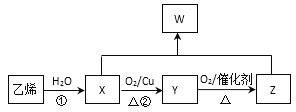
请回答:
(1)乙烯的电子式是_____________
(2)反应①的反应类型是__________
(3)X→Y的方程式是______________________
(4)X+Z→W的方程式是_____________,实验室常用图所示的装置实现这一转化
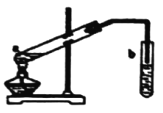
①试管b中一般加入____溶液
②从试管b中分离出W的方法是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关重要。请回答下列问题:
(1)煤的气化。原理是C(s)+2H2(g)![]() CH4(g) ΔH。
CH4(g) ΔH。
在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
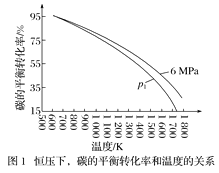

①有关图1、图2的说法正确的有___(填字母)。
a.p1<6MPa b.T1<1000K
c.ΔH<0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=__(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO+H2)与N2的体积之比为3.1~3.2,发生的反应有C(s)+H2O(g)![]() CO(g)+H2(g),C(s)+
CO(g)+H2(g),C(s)+![]() O2(g)
O2(g)![]() CO(g)。从能量角度考虑,通入空气的目的是___。
CO(g)。从能量角度考虑,通入空气的目的是___。
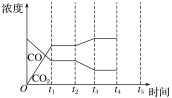
②如图是反应CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
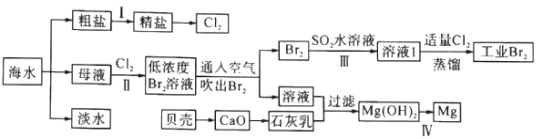
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中依次加入过量BaCl2、Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式:_____________。
(2)海水提溴,制得1mol Br2至少需要消耗_________mol Cl2。步骤Ⅱ中需要向母液中加入稀硫酸酸化,其作用是_________________。步骤Ⅱ若用Na2SO3水溶液吸收Br2,有关反应的离子方程式为__________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2,可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(5)判断Mg(OH)2是否洗涤干净的操作是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PTT纤维综合了尼龙的柔软性、腈纶的蓬松性、涤纶的抗污性,加上本身固有的弹性,以及能常温染色等特点,把各种纤维的优良性能集于一身,从而成为当前国际上最新开发的热门髙分子新材料之一。下面是制备PTT的一种线路:
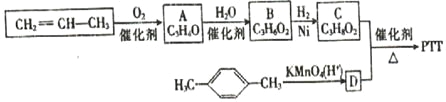
巳知:①A、B、C均为链状化合物,A能发生银镜反应,B结构中含有两种含氧官能团;
②C的核磁共振氢谱表明其有三种不同化学环境的氢,且峰面积之比为1 :2 :1
③1 mol D与足量碳酸氢钠溶液反应可生成2 mol CO2。
(1)B所含官能团的名称是________,A的结构简式是_______.
(2)C的系统名称是_________,写出与C含有相同官能团的C的一种同分异构体的结构简式:_____________。
(3)写出下列反应的反应类型:A→B____________,C+D→PTT_______________.
(4)C与D反应生成PTT的化学方程式是______________________.
(5)分子式为C4H6O且与A互为同系物的同分异构体有_________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式不正确的是
A.向铁制器具上电镀铜,阴极的电极反应为:Cu2++2e-=Cu
B.电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.饱和Na2CO3溶液与CaSO4固体反应:CO32-(aq)+CaSO4(s)![]() CaCO3(s)+SO42-(aq)
CaCO3(s)+SO42-(aq)
D.向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42- =BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:
 +HCl
+HCl
下列有关叙述正确的是
A.I的分子式为C9H10O4
B.II中所有原子有可能均共面
C.可用FeCl3溶液鉴别有机物I和III
D.1 mol产物III与足量溴水反应,消耗Br2的物质的量为1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“烂板液”指的是制印刷锌板时,用稀硝酸腐蚀锌板后得到的“废液”(含有少量Cl-、Fe3+)。某化学兴趣小组用“烂板液”制取Zn(NO3)2·6H2O的过程如图:
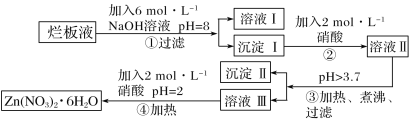
已知:Zn(NO3)2·6H2O是一种无色晶体,其水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂板液”中溶质的主要成分是___(填化学式)。
(2)在操作①中保持pH=8的目的是___。
(3)沉淀Ⅰ的主要成分是___(填化学式)。
(4)操作③中加热煮沸的目的是___;
(5)操作④保持pH=2的目的是___;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)![]() 2Z(g),△H<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量,下列说法中正确的是( )
2Z(g),△H<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量,下列说法中正确的是( )
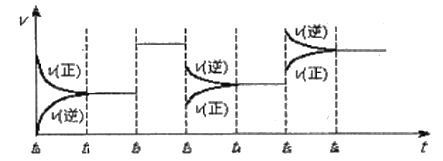
A.t3时降低了温度
B.t2-t3时间段相对于t1-t2时间段来说平衡并没有移动
C.t5时增大了压强
D.t4-t5时间内反应物的转化率最低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com