
某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)取样品a g,称取时使用的仪器名称为托盘天平.
(2)将样品溶于足量稀盐酸中,过滤,滤渣中含有;在溶解过滤时使用的主要仪器有
(3)往滤液中加入过量溶液,过滤,写出该步操作中有关的化学方程式:.
(4)在第(3)步的滤液中通入足量CO2,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g.有关反应的化学方程式为:.
(5)计算该样品中铝的质量分数的表达×100%.
| 探究物质的组成或测量物质的含量. | |
| 专题: | 实验探究和数据处理题. |
| 分析: | (1)称量固体需要的仪器为托盘天平; (2)铝合金(硬铝)中含有镁、铜、硅溶于足量稀盐酸中,过滤,滤渣为铜和硅,滤液为氯化铝、氯化镁,依据溶解过滤装置选择需要的仪器; (3)往滤液中加入过量NaOH溶液,生成偏铝酸钠,氢氧化镁沉淀,过滤得到滤液为偏铝酸钠,沉淀为氢氧化镁; (4)偏铝酸钠溶液中通入过量的二氧化碳生成氢氧化铝沉淀,灼烧得到氧化铝; (5)将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g为氧化铝的质量,结合铝元素守恒计算得到质量分数. |
| 解答: | 解:(1)称量固体需要的仪器为托盘天平,取样品a g,称取时使用的仪器名称为托盘天平,故答案为:托盘天平; (2)铝合金(硬铝)中含有镁、铜、硅溶于足量稀盐酸中,过滤,滤渣为铜和硅,滤液为氯化铝、氯化镁,依据溶解过滤装置选择需要的仪器为漏斗、烧杯、玻璃棒; 故答案为:Cu、Si;漏斗、烧杯、玻璃棒; (3)往滤液中加入过量NaOH溶液,生成偏铝酸钠,氢氧化镁沉淀,过滤得到滤液为偏铝酸钠,沉淀为氢氧化镁,反应的化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl,AlCl3+3NaOH═Al(OH)3↓+3NaCl,Al(OH)3+NaOH═NaAlO2+2H2O; 故答案为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl,AlCl3+3NaOH═Al(OH)3↓+3NaCl,Al(OH)3+NaOH═NaAlO2+2H2O; (4)偏铝酸钠溶液中通入过量的二氧化碳生成氢氧化铝沉淀和碳酸氢钠,灼烧氢氧化铝分解得到氧化铝,发生反应为NaAlO2+CO2+2H2O═NaHCO3+Al(OH)3↓,2Al(OH)3 故答案为:NaAlO2+CO2+2H2O═NaHCO3+Al(OH)3↓,2Al(OH)3 (5)将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g为Al2O3,该样品中铝的质量分数的表达式= |
| 点评: | 本题考查了物质分离提纯的分析判断,主要是实验过程的分析应用,实验基本操作方法和反应离子方程式书写时解题关键,题目较简单. |


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得。A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应:
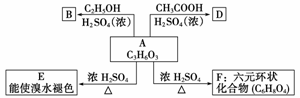
试写出:
化合物的结构简式:
A__________________,B________________________________________________________________________,
D__________________。
化学方程式:A→E:
________________________________________________________________________
________________________________________________________________________,
A→F:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于合成氨的反应,使用催化剂和施加高压,下列叙述中,正确的是( )
A.都能提高反应速率,都对化学平衡状态无影响
B.都对化学平衡状态有影响,都不影响达到平衡状态所用的时间
C.都能缩短达到平衡状态所用的时间,只有压强对化学平衡状态有影响
D.催化剂能缩短反应达到平衡状态所用的时间,而压强无此作用
查看答案和解析>>
科目:高中化学 来源: 题型:
把4.6g钠放入200mL 0.1mol/L的AlCl3溶液中,待其充分反应后,下列叙述中错误的是()
| A. | Cl﹣的浓度几乎不变 | |
| B. | 溶液呈浑浊 | |
| C. | 溶液中几乎不存在Al3+ | |
| D. | 溶液中存在最多的离子是Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,错误的是
A.酸碱中和反应属放热反应
B.化学变化中的能量变化主要由化学键变化引起的
C.煤、石油、天然气是当今世界最重要的三种化石燃料
D.相同条件下,1mol石墨转化为金刚石要吸收1.895kJ热量,说明金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
能够说明苯分子中碳原子间不存在一般单键和双键,而存在完全等同的碳碳键的事实是( )
A.甲苯不存在同分异构体
B.邻二甲苯不存在同分异构体
C.间二甲苯不存在同分异构体
D.对二甲苯不存在同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应2SO2+O2  2SO3,下列判断正确的是
2SO3,下列判断正确的是
A. 2体积SO2和足量O2反应,必定生成2体积SO3
B. 其他条件不变,增大压强,平衡必定向右移动
C. 平衡时,SO2消耗速度必定等于O2的生成速率
D. 平衡时,SO2浓度必定等于O2浓度的两倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com