
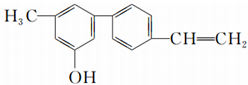
| A. | 该有机物属于烯烃 | B. | 该有机物属于醇 | ||
| C. | 该有机物分子中所有的原子都共面 | D. | 该有机物有两种官能团 |
分析 A.只含C、H元素的有机物属于烃,只含碳碳双键的烃为烯烃;
B.该物质中含有酚羟基,不含醇羟基;
C.乙烯、苯中所有原子共平面,甲烷为正四面体结构,根据乙烯、甲烷和苯的结构判断该分子中所有原子是否共平面;
D.该物质中含有碳碳双键和酚羟基.
解答 解:A.只含C、H元素的有机物属于烃,只含碳碳双键的烃为烯烃,该物质中含有C、H、O三种元素,属于烃的含氧衍生物,故A错误;
B.该物质中含有酚羟基,不含醇羟基,所以不属于醇,故B错误;
C.乙烯、苯中所有原子共平面,该分子中含有甲基,具有甲烷结构特点,所以该分子中所有原子不可能共平面,故C错误;
D.该物质中含有碳碳双键和酚羟基两种官能团,具有烯烃和酚的性质,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃和酚的性质,易错选项是C,注意采用知识迁移方法分析解答.


科目:高中化学 来源: 题型:解答题
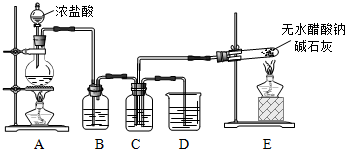
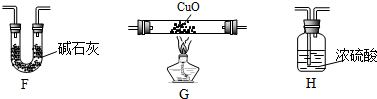
| 装置 | 实验前的质量/g | 实验后的质量/g |
| F | 22.5 | 33.6 |
| H | 42.4 | 51.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红磷转化为白磷,属于物理变化 | |
| B. | 石墨导电、金刚石不导电,故二者不是同素异形体 | |
| C. | O2和O3分子式不同,结构相同 | |
| D. | 单质硫有S2、S4、S6等,它们都是硫的同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
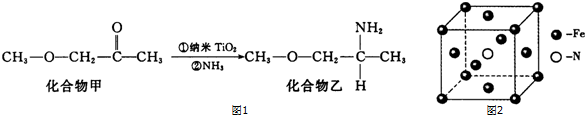
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,4-二甲基己烷 | B. | 2,5-二甲基己烷 | ||
| C. | 4-甲基-2-乙基戊烷 | D. | 2-乙基-4-甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
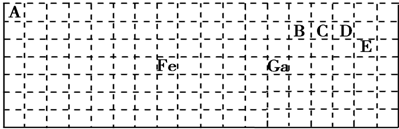
 Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )| A. | 原子半径大小顺序为r(Q)>r(R)>r(T)>r(M)>r(W) | |
| B. | Q、W的单核离子的核外电子数相等 | |
| C. | 五种元素均能形成氢化物 | |
| D. | W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com