
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,工作时反应为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O下列结论正确的是( )
A.Pb为正极被氧化 B.SO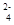 只向PbO2极移动
只向PbO2极移动
C.电解质溶液密度不断减小 D.溶液的pH值不断减小
C
【解析】
试题分析:A.由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,Pb为负极,发生失电子的氧化反应,被还原,故A错误;
B、原电池中阳离子向正极移动,阴离子硫酸根向负极Pb极移动,故B错误;
C、由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,硫酸被消耗,电解质溶液密度不断减小,故C正确;
D、由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,硫酸被消耗,pH不断增大,故D错误.
故选C。
考点:常见化学电源的种类及其工作原理
点评:本题考查原电池的工作原理,题目难度中等,本题注意电极反应式的书写,为解答该题的关键。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学必修二2.2 化学能与电能练习卷(解析版) 题型:选择题
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,工作时反应为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O
下列结论正确的是( )
A.Pb为正极被氧化
B.SO42—只向PbO2极移动
C.电解质溶液密度不断减小
D.溶液的pH值不断减小
查看答案和解析>>
科目:高中化学 来源:2010年陕西省高一第二学期期中考试化学试题 题型:选择题
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论不正确的是
A.Pb为负极被氧化 B.外电路有2 mol电子转移时,负极消耗 SO42-为2 mol
C.溶液的pH不断减小 D.电解质溶液pH不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com