
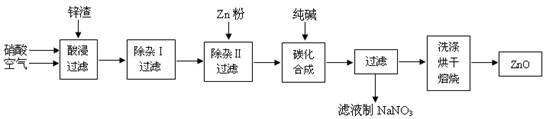
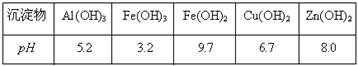


科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
| C.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| D.生铁浸泡在食盐水中发生吸氧腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
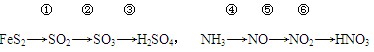
| A.所有变化都是氧化-还原反应 | B.②③⑤⑥都是化合反应 |
| C.两个过程中都有接触室装置 | D.②④反应都要用催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
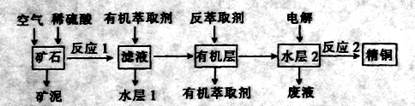
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.硫酸铵 | B.磷酸二氢钙 | C.硫酸钾 | D.尿素 |

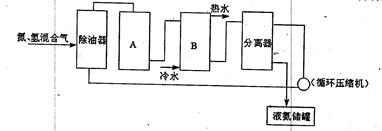
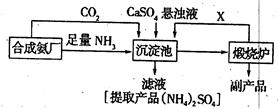
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com