
【题目】有效去除大气中的NOx(主要是NO和NO2)是环境保护的重要课题。
(1)用Pl-g-C3N4光催化氧化法脱除NO的过程如图-1所示。在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应:O2+2H++2e-=H2O2,Pl端的反应:___。

(2)次氯酸盐脱除NO的主要过程如下:
①NO+HClO=NO2+HCl
②NO+NO2+H2O![]() 2HNO2
2HNO2
③HClO+HNO2=HNO3+HCl
下列分析正确的是___。
a.烟气中含有的少量O2能提高NO的脱除率
b.NO2单独存在时不能被脱除
c.脱除过程中,次氯酸盐溶液的pH下降
(3)NaClO溶液能有效脱除NO。25℃时,NO的脱除率随pH的变化如图-2所示;pH=4时,NO的脱除率随温度的变化如图-3所示。
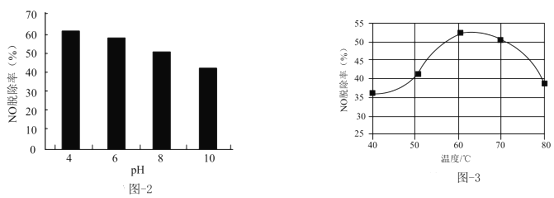
①25℃时,随着pH降低,NO的脱除率增大的原因:___。
②pH=4时,60~80℃NO的脱除率下降的原因:___。
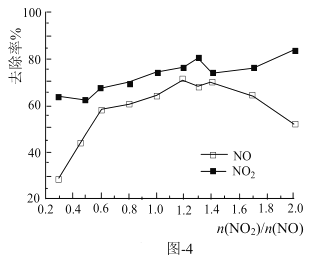
(4)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变![]() ,NOx的去除率如图-4所示。
,NOx的去除率如图-4所示。
已知:NO与Ca(OH)2不反应;
NOx的去除率=1-![]() ×100%
×100%
①![]() 在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___。
在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___。
②当![]() 大于1.4时,NO2去除率升高,但NO去除率却降价。其可能的原因是___。
大于1.4时,NO2去除率升高,但NO去除率却降价。其可能的原因是___。
③O3与NO反应的方程式为:NO+O3=NO2+O2,(该条件下不考虑O2与NO的反应)。保持NO的初始浓度不变,改变n(O3)/n(NO),将反应后的混合气体通入Ca(OH)2悬浊液中吸收。为节省O3的用量,又能保持NOx总去除效果好,则![]() 合适的值范围为___。(保留两位小数)
合适的值范围为___。(保留两位小数)
【答案】NO2e-+H2O=2H++NO2 ac pH降低,ClO-+H+=HClO,溶液中c(HClO)增大 HClO受热分解,溶液中c(HClO)减小 NO+NO2+Ca(OH)2=Ca2++2NO2-+H2O NO2量太多,剩余的NO2和水反应生成NO逸出,导致NO去除率降低 0.55~0.58
【解析】
(1)g-C3N4端得电子,那么Pl端失电子,结合电荷守恒、原子守恒可写P1端离子方程式;
(2)次氯酸盐脱除NO的主要过程可看出,脱NO的本质是转换成HNO3;
(3)NaClO脱NO的过程可看出,实际上是HClO与NO反应,所以pH变化HClO跟着变化,脱NO效果也会跟着变化;
(4)NO和Ca(OH)2不反应,NO、NO和Ca(OH)2三者反应,分析化合价可知产物为亚硝酸钙,在此基础上分析解答。
(1)g-C3N4端得电子发生还原反应,生成过氧化氢,P1端NO失电子变成NO2,这样左边就出现了正电荷,右边加H+,结合原子守恒,左边应加H2O,所以P1端的离子方程式为:NO2e-+H2O=2H++NO2,故答案为:NO2e-+H2O=2H++NO2;
(2)a.从给出的条件看,次氯酸盐脱除NO是先将一部分NO氧化成NO2才脱出的,O2和NO反应生成NO2,就省了第一步了,所以烟气中含有的少量O2能提高NO的脱除率,a正确;
b.从原理上看,氮氧化物转换为HNO3就被脱出了,NO2单独存在时能和水反应生成HNO3和NO,有一定的脱出率,b错误;
c.次氯酸盐水解显碱性,从原理来看,最后生成硝酸和HCl,pH下降,c正确;
故答案为:ac;
(3)①pH降低,c(H+)增大,产生更多的HClO,所以NO的脱除率增大,故答案为:pH降低,ClO-+H+=HClO,溶液中c(HClO)增大;
②HClO会分解,温度太高,HClO分解得太多,溶液中HClO浓度减小了,故答案为:HClO受热分解,溶液中c(HClO)减小;
(4)①NO和Ca(OH)2不反应,所以反应物有NO、NO2和Ca(OH)2,根据氧化还原规律,产物为Ca(NO2)2和水,所以离子方程式为:NO+NO2+Ca(OH)2=Ca2++2NO2-+H2O,故答案为:NO+NO2+Ca(OH)2=Ca2++2NO2-+H2O;
②当![]() 太大,NO2量太多,吸收不完,有一部分NO2就和水反应生成硝酸和NO,这样就导致NO2去除率升高,但NO去除率却降价,故答案为:NO2量太多,剩余的NO2和水反应生成NO逸出,导致NO去除率降低;
太大,NO2量太多,吸收不完,有一部分NO2就和水反应生成硝酸和NO,这样就导致NO2去除率升高,但NO去除率却降价,故答案为:NO2量太多,剩余的NO2和水反应生成NO逸出,导致NO去除率降低;
③从图上看NOx总去除效果最好时,![]() 介于1.2到1.4之间,设NO的物质量为1,那么则NO2的物质的量为1.2介于1.4之间,由NO+O3=NO2+O2可知,此时消耗O3和NO的量均为1.2到1.4之间,所以O3的量为1.2-1.4,NO的量为(1.2+1)到(1.4+1)之间,即
介于1.2到1.4之间,设NO的物质量为1,那么则NO2的物质的量为1.2介于1.4之间,由NO+O3=NO2+O2可知,此时消耗O3和NO的量均为1.2到1.4之间,所以O3的量为1.2-1.4,NO的量为(1.2+1)到(1.4+1)之间,即![]() 在
在![]() 到
到![]() ,即0.55到0.58之间,故答案为:0.55~0.58。
,即0.55到0.58之间,故答案为:0.55~0.58。


科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法中,不正确的是( )
A.一定条件下,2.3 g Na与O2完全反应生成3.6 g产物时失去的电子数0.1NA
B.电解精炼铜时,当电路中转移NA个电子,阳极溶解32 g铜
C.向仅含0.2 mol FeI2的溶液中持续通入氯气,当有0.1 mol Fe2+被氧化时,转移电子的数目为0.5NA
D.标准状况下,锌与某浓度的H2SO4反应生成11.2 L气体,反应中转移的电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯甲烷等卤代烃跟苯的反应如图所示,(无机小分子产物略去)。下列说法正确的是

A. 该反应属于化合反应
B. b的二氯代物有6种结构
C. 1mol b加氢生成饱和烃需要6molH2
D. C5H11Cl的结构有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚碳酸酯(简称PC)是重要的工程塑料,某种PC塑料(N)的合成路线如下:
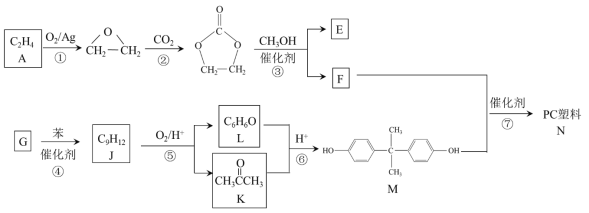
已知:R1COOR2 + R3OH![]() R1COOR3 + R2OH
R1COOR3 + R2OH
(1)①的反应类型是_______________。 K中含有的官能团名称是_______________。
(2)E的名称是_______________。
(3)④是加成反应,G的核磁共振氢谱有三种峰,G的结构简式是__________________。
(4)⑦的化学方程式是______________________________________________。
(5)⑥中还有可能生成分子式为C9H12O2产物。分子式为C9H12O2且符合下列条件的同分异构体共有__________ 种。写出其中两种核磁共振氢谱有5组峰的物质的结构简式_______________________________
a.属于芳香化合物 ,且苯环上只有两个取代基 b.1mol该物质能消耗1molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L的恒容密闭容器中发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH,若起始时充入0.4molCH4和0.4molCO2,测得CH4的平衡转化率与温度的关系如图中曲线a所示。下列说法一定正确的是( )
2CO(g)+2H2(g)ΔH,若起始时充入0.4molCH4和0.4molCO2,测得CH4的平衡转化率与温度的关系如图中曲线a所示。下列说法一定正确的是( )

A.ΔH>0
B.延长M点的反应时间,可以提高CH4的平衡转化率
C.T1℃,起始时若向该容器中充入等物质的量的CH4、CO2、CO和H2,则此时反应向正反应方向进行
D.曲线b可表示向该容器中充入0.5molCH4和0.5molCO2,CH4的平衡转化率与温度的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:
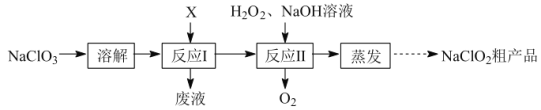
已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
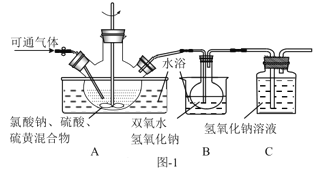
①若X为硫磺与浓硫酸,也可反应生成ClO2。该反应较剧烈。若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
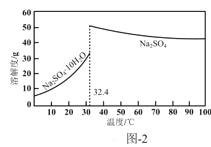
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图2所示。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知P4单质的结构如下,P4在 KOH 溶液中的变化是:P4 + 3KOH + 3H2O = 3KH2PO2 + PH3 ↑,下列说法正确的是( )
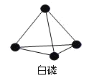
A.产物 PH3分子中所有的原子可能共平面
B.31gP4含有 1.5NA个 P P 键
C.相关元素的电负性大小顺序:P > O > H > K
D.P4中 P 原子为 sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知金刚石中C—C键能小于C60中C—C键能,有同学据此认为C60的熔点高于金刚石,认为此说法是否正确__(填“正确”或“不正确”),并闸述理由__。
(2)格式试剂RMgX(R表示烃基、X表示卤素)遇水剧烈反应,生成可燃性烃RH和__。
(3)64g自燃性气体SiH4在25℃、101Kpa下充分完全燃烧生成液态水和固态氧化物时放出akJ热量,写出该自燃性气体燃烧热的热化学方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com