
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
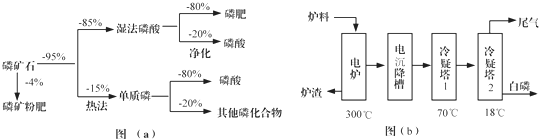
分析 (1)由图(a)可知生产含磷肥料,约占磷矿石使用量的比例为:4%+96%×85%×80%=69%;
(2)以磷矿石为原料,用过量的硫酸溶解Ca5F(PO4)3可制得磷酸,根据质量守恒书写化学方程式;根据P元素守恒可得关系式P2O5~2H3PO4,依据此关系式计算;
(3)将SiO2、过量焦炭与磷灰石混合,高温除了反应生成白磷之外,得到的难溶性固体是CaSiO3;根据冷却塔1、2的温度与白磷的熔点比较分析白磷的状态;
(4)二氧化硅和HF反应生成四氟化硅气体,过量的焦炭不完全燃烧生成CO,因此在尾气中主要含有SiF4、CO,还含有少量的PH3、H2S和HF等;将尾气通入纯碱溶液,SiF4、HF、H2S与碳酸钠反应而除去,次氯酸具有强氧化性,可除掉强还原性的PH3;
(5)相比于湿法磷酸,热法磷酸工艺所得产品纯度大.
解答 解:(1)由图(a)可知生产含磷肥料,约占磷矿石使用量的比例为:4%+96%×85%×80%=69%,
故答案为:69;
(2)以磷矿石为原料,用过量的硫酸溶解Ca5F(PO4)3可制得磷酸,根据质量守恒定律可得反应的化学方程式为Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑;
根据P元素守恒可得关系式P2O5~2H3PO4,142份P2O5可制取196份磷酸,1t折合含有P2O5约30%的磷灰石,含有P2O5的质量为0.3t,所以可制得到85%的商品磷酸的质量为$\frac{196×0.3t}{142×85%}$=0.49t,
故答案为:Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑;0.49;
(3)将SiO2、过量焦炭与磷灰石混合,高温除了反应生成白磷之外,得到的难溶性固体是CaSiO3;冷却塔1的温度是70℃,280.5℃>t>44℃,所以此时主要的沉积物是液态白磷;冷却塔2的温度是18℃,低于白磷的熔点,故此时的主要沉积物是固体白磷,
故答案为:CaSiO3;液态白磷;固态白磷;
(4)二氧化硅和HF反应生成四氟化硅气体,过量的焦炭不完全燃烧生成CO,因此在尾气中主要含有SiF4、CO,还含有少量的PH3、H2S和HF等;将尾气通入纯碱溶液,SiF4、HF、H2S与碳酸钠反应而除去,次氯酸具有强氧化性,可除掉强还原性的PH3,
故答案为:SiF4、CO;SiF4、H2S、HF;PH3;
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但是所得产品纯度大,杂质少,因此逐渐被采用,
故答案为:产品纯度高.
点评 本题考查了制备方案的设计,题目难度中等,涉及磷矿石的主要用途、反应原理和有关计算,该题是高考中的常见题型,试题综合性强,侧重对学生分析问题、解答问题能力的培养和解题方法的指导,明确实验目的、实验原理为解答关键.


科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 用干燥洁净的玻璃棒蘸取待测溶液,滴在pH试纸上,再跟标准比色卡比较得到该溶液的pH值 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3NO2+H2O═2HNO3+NO | B. | 4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2 | ||
| C. | 3Cl2+8NH3═N2+6NH4Cl | D. | 2Na+2NH3(液)═2NaNH2+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
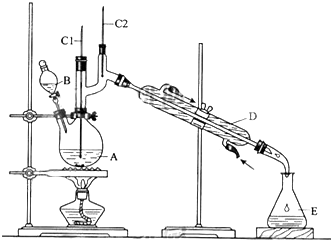
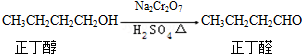
| 沸点/℃ | 密度(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
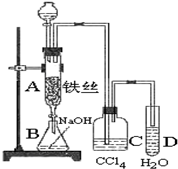 实验室用图装置制取少量溴苯,试填写下列空白.
实验室用图装置制取少量溴苯,试填写下列空白.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
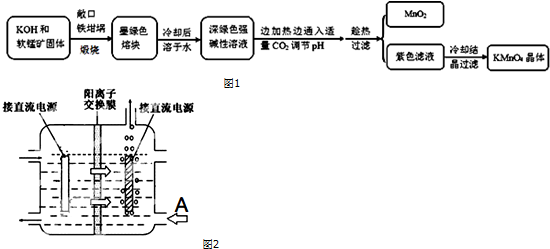
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
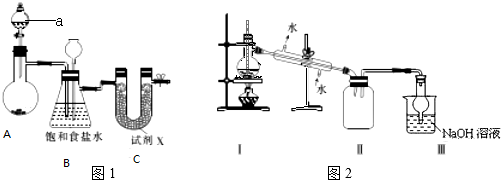
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
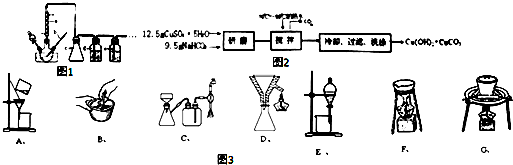
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com