
200��ʱ��11.6 g CO2��ˮ�����Ļ�������������Na2O2��ַ�Ӧ��������������3.6 g���ٽ���Ӧ��ʣ�������ȴ����뺬�� ��
�� ��
�� ��
�� �����ӵ�ˮ��Һ�У�����Һ������ֲ��䣬������˵������ȷ����
(����)
�����ӵ�ˮ��Һ�У�����Һ������ֲ��䣬������˵������ȷ����
(����)
A��ԭ��������ƽ��Ħ������Ϊ23.2 g/mol
B�����������Na2O2��Ӧ�����е���ת�Ƶ����ʵ���Ϊ0.25 mol
C����Һ�� �����ʵ���Ũ�Ȼ������ֲ���
�����ʵ���Ũ�Ȼ������ֲ���
D����Һ�� �����ʵ���Ũ�ȼ�С��
�����ʵ���Ũ�ȼ�С�� �����ʵ���Ũ��������
�����ʵ���Ũ�������� ��
�� �����ʵ���Ũ��֮�ͻ������ֲ���
�����ʵ���Ũ��֮�ͻ������ֲ���
A
��������
���������A���������CO2��H2O�����ʵ����ֱ�Ϊm��n
��44m+18n=11.6��
1mol��CO2��1mol��H2O��Na2O2��Ӧ�����������ֱ����ӣ�44-16��=28g����18-16��=2g
����28m+2n=3.6��
�ϲ��٢�
���m=0.1mol n=0.4mol
M(ƽ��)=m(��)/n(��)=11.6g/(0.1mol+0.4mol)= 23.2 g/mol��A��ȷ��
B�2CO2 + 2Na2O2 = 2Na2CO3 + O2�٣�2Na2O2+2H2O="==4NaOH+" O2���ڣ�����ת�Ƶ���0.1mol������ת�Ƶ���0.4mol����ת�Ƶ�����Ϊ0.5mol��B����
C��D�ʣ�������뵽��Һ�У�OH-��HCO3-������Ӧ��OH-+ HCO3-=CO32-+H2O�ۣ���Һ��HCO3-Ũ�ȼ��٣�CO32-Ũ��������Դ2�����棬ʣ�����Na2CO3�еĺͷ�Ӧ�۵ģ� ��
��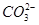 �����ʵ���Ũ��֮�ͻ�����
�����ʵ���Ũ��֮�ͻ�����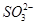 ˮ�ⷽ��ʽΪ��
ˮ�ⷽ��ʽΪ��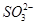 +H20
+H20 HSO32-+OH-�ܣ�ʣ�����NaOH���뵽��Һ�л��д�����OH-����Ӧ�ܻ������ƶ���
HSO32-+OH-�ܣ�ʣ�����NaOH���뵽��Һ�л��д�����OH-����Ӧ�ܻ������ƶ���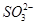 Ũ�Ȼ�����C��D����ѡA��
Ũ�Ȼ�����C��D����ѡA��
���㣺��ѧ����
��������������ݲ��൫�������������Ƶ����ʣ�ˮ�ⷴӦ�����ƶ����dz�����֪ʶ�㡣


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
200 ��?ʱ��11.6 g CO2��ˮ�����Ļ��������������Na2O2��ַ�Ӧ����Ӧ����������������3.6 g����ԭ��������ƽ����Է�������Ϊ(����)
A.5.8 B.11.6?
C.23.2 D.46.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�찲��ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
200��ʱ��11.6 g CO2��H2O�Ļ����������������Na2O2��Ӧ����Ӧ�����������3.6 g����ԭ������ƽ����Է�������Ϊ
A��5.8 B��11.6 C��23.2 D��46.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���㽭��һ�и�����ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
200��ʱ��11.6 g CO2��ˮ�����Ļ�������������Na2O2��ַ�Ӧ��������������3.6 g���ٽ���Ӧ��ʣ������ܷ���ȴ����뺬��Na����HCO��SO��CO�����ӵ�ˮ��Һ�У�����������Һ������ֲ��䣬������˵������ȷ����
A��ԭ���������CO2��ˮ������0.25mol
B�����������Na2O2��Ӧ�����е���ת�Ƶ����ʵ���Ϊ0.50 mol
C����Һ��SO�����ʵ���Ũ�Ȼ������ֲ���
D����Һ��HCO�����ʵ���Ũ�ȼ�С��CO�����ʵ���Ũ��������HCO��CO�����ʵ���Ũ��֮�ͻ������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡ������ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
200��ʱ��11.6 g CO2��H2O�Ļ����������������Na2O2��Ӧ����Ӧ�����������3.6 g����ԭ������ƽ����Է�������Ϊ �� ��
A��5.8 B��11.6 C��23.2 D��46.4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com