
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
对于反应3Cl2+6NaOH 5NaCl+NaClO3+3H2O,以下叙述正确的
5NaCl+NaClO3+3H2O,以下叙述正确的 是
是
A.Cl2是氧化剂,NaOH是还原剂
B.当有6.72L Cl2反应时,转移电子物质的量为0.5mol
C.氧化剂得电子总数与还原剂失电子总数之比为1∶1
D.被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
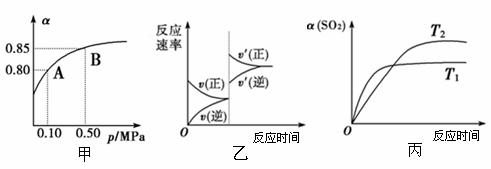
已知反应:2SO2(g)+O2(g) 2SO3(g) 。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)、温度(T)的关系分别如图甲、丙所示。
2SO3(g) 。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)、温度(T)的关系分别如图甲、丙所示。
则下列说法正确的是
A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.由图丙知,T1>T2,且该反应的正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
今有下列三个氧化还原反应:
①2FeCl3+2KI===2FeCl2+2KCl+I2
②2FeCl2+Cl2===2FeCl3
③2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O
若某溶液中有Fe2+、I-、Cl-共存,要除去I-而不氧化Fe2+和Cl-,则可加入的试剂是
A.Cl2 B.KMnO4 C.HCl D.FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将该温度下a mL pH=13 NaOH溶液与b mL0.05mol/L H2SO4混合,所得混合溶液的pH=7,
则a:b =
(2)若在含有足量AgCl固体的饱和AgCl溶液中分别放入:A、100mL蒸馏水中;B、100mL 0.2 mol·L-1AgNO3溶液中;C、100 mL 0.1 mol·L-1AlCl3溶液中;D、100mL 0.1 mol·L-1盐酸溶液中。充分搅拌后,银离子浓度最小的是 (填序号)
(3)在25℃下,向浓度均为0.20 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
沉淀(填化学式),生成该沉淀的离子方程式为 ;当测得溶液pH=11.00时,则此温度下残留在溶液中的c(Mg2+):c(Cu2+)=
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.0×10-20)
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,请参照①~⑥在表中的位置,用化学用语回答下列问题:
| I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ |
(1) ⑥有两种同位素,其中一种原子核内有18个中子,其原子符号为_______;
(2)②与④可以形成一种温室气体,其电子式为_______;
(3) ③和⑤的氢化物沸点 __________(填分子式)高,原因是______________;
(4)②和⑥按原子个数比为1:4形成的化合物为_______分子(填极性或非极性),含有_______键(填极性或非极性)
(5) ②形成的单质可以是不同类型的晶体,它们可能是____________(填字母)
A原子晶体 B分子晶体 C金属晶体 D离子晶体 E混合型晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是( )
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质化合生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源: 题型:
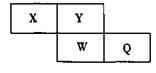
短周期元素X、Y、W、Q在元素周期表中的相对位置如右下图所示。Y是地壳中含量最多的元素。下列说法正确的是( )
A.1mol Q单质与氢氧化钠溶液反应转移的电子数目为2 NA
B.X的气态氢化物能使湿润的蓝色石蕊试纸变红
C.氢化物的沸点:H2Y>HQ
D.最髙价氧化物的水化物的酸性:W > Q
查看答案和解析>>
科目:高中化学 来源: 题型:
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示,遇水易水解,并产生能使品红褪色的气体。S2Br2与S2Cl2结构相似。下列说法错误的是
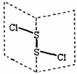
A.S2Cl2中硫原子轨道杂化类型为sp3杂化
B.S2Cl2为含有极性键和非极性键的非极性分子
C.熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:2 S2Cl2 + 2 H2O = SO2↑ + 3 S↓ + 4 HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com