
 X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2;U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题:
X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2;U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题: .
.分析 X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子,则Y为N元素;U是第三周期元素形成的简单离子中半径最小的元素,则U为Al;X、Z中未成对电子数均为2,X的原子序数小于N,而Z的原子序数介于N、Al之间,X、Z的核外电子排布分别为1s22s22p2,1s22s22p4,故X为C元素、Z为O元素;W的内层电子全充满,最外层只有1个电子,原子序数大于Al,只能处于第四周期,核外电子数为2+8+18+1=29,故W为Cu元素,据此解答.
解答 解:X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子,则Y为N元素;U是第三周期元素形成的简单离子中半径最小的元素,则U为Al;X、Z中未成对电子数均为2,X的原子序数小于N,而Z的原子序数介于N、Al之间,X、Z的核外电子排布分别为1s22s22p2,1s22s22p4,故X为C元素、Z为O元素;W的内层电子全充满,最外层只有1个电子,原子序数大于Al,只能处于第四周期,核外电子数为2+8+18+1=29,故W为Cu元素.
(1)同周期随原子序数增大,第一电离能呈增大趋势,但N元素2p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能N>O>C,
故答案为:N>O>C;
(2)W为Cu元素,价电子排布式为3d104s1,价电子排布图为: ,
,
故答案为: ;
;
(3)根据等电子体原理,可知化合物CO与N2互为等电子体,CO的结构式是C≡O,
故答案为:C≡O;
(4)X、Y、Z的最简单氢化物分别为CH4、NH3、H2O,3种氢化物的中心原子价层电子对数均为4,VSEPR模型均为正四面体形,但中心原子的孤电子对数依次增大,导致键角变小,故键角:CH4>NH3>H2O,
故答案为:CH4>NH3>H2O;3种氢化物的中心原子价层电子对数均为4,VSEPR模型均为正四面体形,但中心原子的孤电子对数依次增大,导致键角变小;
(5)晶胞中N原子数目为4,Al原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故该化合物化学式为AlN,Y原子形成4个共价键,故Y原子杂化方式为sp3,
故答案为:AlN;sp3;
(6)设晶胞中Al原子数目为N(Al),则N(Al)×$\frac{27}{6.02×1{0}^{23}}$g=(405×10-10)3×2.70g/cm3,解得N(Al)=4.00,所以其晶胞的类型面心立方密堆积,
故答案为:面心立方最密堆积.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、电离能、杂化方式、晶胞计算等,是对学生综合能力的考查,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 ,其化学键的类型为离子键、共价键.
,其化学键的类型为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)
;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
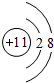 .
.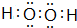 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性Cl-、Br-、I- | B. | 碱性:Na0H、Mg(OH)2、Al(OH)3 | ||
| C. | 稳定性HCl、H2S、PH3 | D. | 酸性:HC1O4、H2SO4、H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com