
A、碳-12原子
| ||
B、氟化钠的电子式 | ||
| C、硫离子的核外电子排布式 1s22s22p63s23p4 | ||
D、甲烷的电子式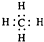 |
12 6 |
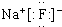 ,故B错误;
,故B错误;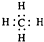 ,故D正确;
,故D正确;

科目:高中化学 来源: 题型:
| A、常温下浓硝酸能使铝发生钝化,可在常温下用铝制贮藏贮运浓硝酸 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、ClO2具有还原性,可用于对自来水的杀菌消毒 |
| D、铜的金属活泼性比铁的差,所以氯化铁溶液不能溶解铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L Na2CO3溶液中:c(Na+)+c(H+)═c(CO32-)+c(HCO3-)+c(OH-) |
| B、向CH3COONa溶液中加入适量的CH3COOH,得到pH=4的混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、在等物质的量浓度的四种溶液①NH4Cl②CH3COONH4③NH4HSO4④NH3?H2O中,NH4+浓度大小顺序正确的是③>①>②>④ |
| D、0.1mol/L Na2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向碳酸氢钙溶液中滴加少量氨水:Ca2++HCO3-+NH3?H2O═CaCO3↓+H2O+NH4+ |
| B、二氧化硫气体通入棕黄色的氯化铁溶液中,棕黄色褪去:2Fe3++SO2+H2O═SO42-+2Fe2++2H+ |
| C、向氯化钙溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| D、向硫酸氢钠溶液中滴入氢氧化钡溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、②③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与硫酸铜溶液反应:2Na++Cu═Cu2++2Na+ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
| D、将氯气通入足量的氯化亚铁溶液中:Cl2+2Fe2+═2Cl-+2Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、温度计插入到反应物液面以下 |
| B、生成的乙烯混有刺激性气味的气体 |
| C、反应过程中溶液的颜色会逐渐变黑 |
| D、加热时要注意使温度缓慢上升至170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质A由Z与Y两种元素组成,则0.5mol物质A中含有的离子数约为9.03×1023 |
| B、元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大 |
| C、元素Z、R的氧化物的水化物之间相互反应生成的盐溶液呈中性或碱性 |
| D、元素Y、R分别与元素X形成的化合物的沸点:XmY<XmR |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com